- ПОВЕРХНОСТНО-АКТИВНЫЕВЕЩЕСТВА
- ПОВЕРХНОСТНО-АКТИВНЫЕВЕЩЕСТВА
-
- (ПАВ) - вещества (как правило, органич. соединения), обладающие высокой поверхностной активностью, т. е. способностью адсорбироваться на межфазных границах и сильно снижать поверхностное натяжение. Мерой поверхностной активности может служить значение производной
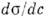 при с
при с 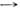 0, где
0, где 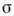 - поверхностное натяжение, с - объёмная концентрация ПАВ. В принципе любое вещество в определённых условиях может проявить поверхностную активность. В особый класс ПАВ выделяются вещества, имеющие высокую поверхностную активность на границах водного раствора.
- поверхностное натяжение, с - объёмная концентрация ПАВ. В принципе любое вещество в определённых условиях может проявить поверхностную активность. В особый класс ПАВ выделяются вещества, имеющие высокую поверхностную активность на границах водного раствора.
Поверхностная активность обусловлена строениеммолекул ПАВ: они дифильны, т. е. содержат одновременно гидрофильную (полярную)и гидрофобную (липофильную) атомные группы (см. Гидрофильность и гидрофобностъ). В качестве гидрофильных могут выступать функциональные группы спиртов( - ОН), кислот ( - СООН, - S03H, - S04H и др.) иих солей, аминов( - ГШ 2) и др. группы. Липофильные группы обычнопредставлены углеводородными или фторуглеродными радикалами.
Одна молекула ПАВ может содержать неск. <групп обоих видов. Для того чтобы ПАВ собиралось преим. на границе фаз(а не внутри одной из них), гидрофильная и липофильная части молекулы должныбыть энергетически сбалансированы. Соответствующая количеств. характеристика- число гидрофильно-липофильного баланса (ГЛБ) по шкале Гриффина - Дэвисазадаётся соотношением ГЛБ = 7 + 0,36 W/kT, где W - работапереноса 1 молекулы ПАВ из полярной в неполярную фазу (обычно из воды вжидкий углеводород). Для большинства ПАВ числа ГЛБ находятся в интервале0 - 40. Малые числа ГЛБ соответствуют маслорастворимым, большие - водорастворимымПАВ. Числа ГЛБ обладают свойством аддитивности по отношению к отд. группаммолекулы ПАВ. Имеются таблицы групповых чисел, по к-рым быстро рассчитываетсячисло ГЛБ для любого соединения. Число ГЛБ определяет назначение и эффективностьдействия ПАВ.
Наиб. важной классификацией ПАВ являетсяклассификация по ионогенным свойствам гидрофильных групп: 1) анионные (апионактивные)ПАВ, способные диссоциировать в полярном растворителе с образованием поверхностно-активныханионов - соли карбоновых кислот (в т. ч. мыла), алкилсульфаты, алкилсульфонаты, <алкиларплсульфонаты, фторуглеродные сульфонаты и др.; 2) катионные (катионеактивные)ПАВ, способные диссоциировать с образованием поверхностно-активных катионов(производные алкиламипов и др.); 3) амфотерные (амфолитные) ПАВ, содержащиенеск. полярных групп и дающие при диссоциации, в зависимости от величины рН в водном растворе поверхностно-активные анионы или катионы; 4)цвиттер-ионные ПАВ, в нейтральных полярных группах к-рых противоположныезаряды существенно разделены в пространстве др. структурными элементамимолекулы [напр., бетаины состава RN+(CH2C6H5)(GH3) СН 2 СОО -, где R - алкил с числоматомов углерода 8 - 12); 5) неионные (неионогенные) ПАВ с протяжённой полярнойгруппой - полиоксиэтиленовые эфиры алифатич. спиртов и кислот, алкилфенолов, <аминов и др. соединений. Первые 3 типа часто объединяются под общим назв. <ионных (ионогенных) ПАВ. Наиб. распространены анионные и неионные ПАВ. <Поверхностно-активные вещества также делятся на низко- и высокомолекулярные(с периодич. расположением гидрофильных и липофильных групп в линейнойполимерной цепи), масло- и водорастворимые, коллоидные (мицеллообразующие, <их отличает оптимальная величина ГЛБ) и неколлоидные. Др. направление классификации- по назначению ПАВ. Различают эмульгаторы (ГЛБ 3,5 - 6 и 8 - 18), смачиватели(7 - 9), моющие агенты (детергенты, 13 - 15), солюбилизаторы (15 - 18)и т. д.
Адсорбция ПАВ при малой объёмной концентрацииносит мономолекулярный характер (см. Мономолекулярный слой )и сопровождаетсявозникновением поверхностного давления. Кинетика адсорбции определяетсяскоростью диффузии и для нек-рых ПАВ специфич. энергетич. барьером адсорбции, <связанным с молекулярным строением ПАВ. Равновесная мономолекулярная адсорбцияодного ПАВ описывается ур-нием Ленгмюра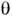 =kc/(1+ kc), где
=kc/(1+ kc), где 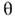 - степень заполнения монослоя, с - концентрация ПАВ в объёмной фазе,k- постоянная для данного вещества величина. На межфазной границе молекулыПАВ располагаются так, что гидрофильная группа остаётся в фазе, состоящейиз полярных молекул. При адсорбции из водных растворов большую рольиграет гидрофобный эффект - стремление воды к ликвидации внутр. полостейи выталкиванию гидрофобных тел, обусловленное межмолекулярным взаимодействиеми структурой воды. Благодаря гидрофобному эффекту липофильные углеводородныеили фторуглеродные цепи молекул ПАВ выталкиваются из водного раствора ввоздух, соседнюю жидкую фазу из неполярных молекул или прижимаются к поверхноститвёрдого тела. На границе раствор - воздух цепи ориентируются при малых
- степень заполнения монослоя, с - концентрация ПАВ в объёмной фазе,k- постоянная для данного вещества величина. На межфазной границе молекулыПАВ располагаются так, что гидрофильная группа остаётся в фазе, состоящейиз полярных молекул. При адсорбции из водных растворов большую рольиграет гидрофобный эффект - стремление воды к ликвидации внутр. полостейи выталкиванию гидрофобных тел, обусловленное межмолекулярным взаимодействиеми структурой воды. Благодаря гидрофобному эффекту липофильные углеводородныеили фторуглеродные цепи молекул ПАВ выталкиваются из водного раствора ввоздух, соседнюю жидкую фазу из неполярных молекул или прижимаются к поверхноститвёрдого тела. На границе раствор - воздух цепи ориентируются при малых 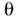 горизонтально, при больших - вертикально.
горизонтально, при больших - вертикально.
Мицеллы ПАВ - молекулярные или ионныеагрегаты размером ок. 3 - 100 нм, возникающие в растворах коллоидных ПАВпо достижении критич. концентрации мицеллообразования. Мицеллярные растворыПАВ обладают специфич. свойствами. Переход к мицеллообразованию происходитв узком интервале концентраций, и его можно трактовать как фазовый переход2-го рода. Причиной мицеллообразования в водных растворах является гидрофобныйэффект, а в средах из неполярных молекул - взаимное притяжение полярныхгрупп молекул ПАВ. При приближении концентрации ПАВ к критич. концентрациимицеллообразования происходит резкое изменение свойств раствора: электропроводности, <поверхностного натяжения, коэф. рассеяния света, осмотич. давления, коэф. <диффузии и т. д. Ниже определённой темп-ры (точки Крафта) образование мицеллне происходит, а при увеличении концентрации ПАВ наблюдается кристаллизация. <Кривая равновесия мицеллярного раствора с твёрдой фазой на диаграмме состоянияназ. границей Крафта. Её верхний предел соответствует нижней темп-ре существованияжидких кристаллов, образование к-рых характерно для концентрпров. растворовПАВ. Для мицелл характерен полиморфизм: при повышении концентрации ПАВформа мицелл переходит от сферической к цилиндрической (стержпеобразной),а затем - к пластинчатой (дискообразной).
Мицеллярные растворы могут растворятьвещества, малорастворимые в данном растворителе, этот процесс наз. солюбилизацией. <Он состоит в проникновении молекул растворимого вещества в мицеллы. Солюбилизацияможет происходить не только из соседней фазы, но и из собств. адсорбционногослоя раствора. На этом основан метод обнаружения в ПАВ поверхностно-активныхпримесей: ниже критич. концентрации мицеллообразования они в большой концентрациинаходятся в адсорбционном слое и поверхностное натяжение падает с увеличениемконцентрации раствора, выше этой концентрации - переходят в мицеллы и поверхностноенатяжение возрастает. Т. о., наличие минимума на изотерме поверхностногонатяжения раствора ПАВ свидетельствует о примесях в ПАВ.
ПАВ оказывают стабилизирующее действиев эмульсиях и др. дисперсных системах (суспензиях, пенах).
Применение ПАВ многообразно и продолжаетрасширяться. ПАВ используются как моющие средства, ингибиторы коррозии, <смачиватели, плёнкообразователи, пенообразователи, пеногасители, эмульгаторы, <диспергаторы, регуляторы роста кристаллов. Известны применения ПАВ в процессахфлотации, для повышения отдачи нефтяных пластов, сборки нефти, борьбы сугольной пылью, гашения волн и турбулентностей, замедления испарения водоёмов, <придания водоотталкивающих свойств почвам, цементам и др. материалам. ДобавкиПАВ повышают качество строит. материалов, смазок и металлорежущего инструмента. <ПАВ необходимы для производства хим., пищевых, лекарственных эмульсий, <пен (пожарных пен, пенопластов, пенобетонов и т. п.), аэрозолей и др.Лит.: Абрамзон А. А., Поверхностно-активныевещества, 2 изд., Л., 1981; Русанов А. И., Левичев С. А., Жаров В. Т.,Поверхностное разделение веществ, Л., 1981.
А. И. Русанов.
Физическая энциклопедия. В 5-ти томах. — М.: Советская энциклопедия. Главный редактор А. М. Прохоров. 1988.
.
