- ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ
- ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ
-
- один из осн. законов термодинамики, устанавливающий необратимость реальных термодинамич. процессов. В. н. т. сформулировано как закон природы H. Л. С. Карно (N. L. S. Carnot) в 1824, P. Клаузиусом (R. Clausius) в 1850 и У. Томсоном (Кельвином) (W. Thomson, Kelvin) в 1851 в различных, но эквивалентных формулировках. В. н. т. в формулировке Клаузиуса утверждает, что процесс, при к-ром не происходит никаких изменений, кроме передачи тепла от горячего тела к холодному, необратим, т. е. теплота не может самопроизвольно переходить от более холодного тела к более горячему (принцип Клаузиуса). Согласно формулировке Томсона, процесс, при к-ром работа переходит в тепло без к.-л. иных изменений состояния системы, необратим, т. е. невозможно полностью преобразовать в работу всё тепло, взятое от тела, не производя никаких др. изменений состояния системы (принцип Tомсона). Принцип Томсона эквивалентен утверждению о невозможности вечного двигателя2-го рода. В. н. т. можно сформулировать также в виде принципа Каратеодори: вблизи любого состояния термодинамич. равновесия и сколь угодно близко к нему существует состояние, в к-рое нельзя попасть при помощи адиабатич. процесса.
Из невозможности вечного двигателя 2-го рода следует Карно теорема о том, что кпд любого теплового двигателя не превосходит кпд Карно цикла
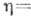
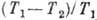 ., к-рый определяется только темп-рой нагревателя T1 и холодильника T2. На основании теоремы Карно удаётся построить абс. шкалу темп-р (шкалу Кельвина, см. Абсолютная температура).
., к-рый определяется только темп-рой нагревателя T1 и холодильника T2. На основании теоремы Карно удаётся построить абс. шкалу темп-р (шкалу Кельвина, см. Абсолютная температура).
Рассматривая циклич. процесс, при к-ром система получает (или от неё отнимают) малые кол-ва теплоты dQ при абс. темп-ре T, можно сформулировать В. н. т. в виде Клаузиуса неравенства

интеграл берётся по замкнутому циклу; если тепло отнимают, то считается, что
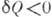 . Знак равенства относится к обратимым процессам (равенство Клаузиуса). Клаузиус установил неравенство (1), рассматривая циклич. процесс как предел суммы большого числа элементарных циклов Карно.
. Знак равенства относится к обратимым процессам (равенство Клаузиуса). Клаузиус установил неравенство (1), рассматривая циклич. процесс как предел суммы большого числа элементарных циклов Карно.
Из равенства Клаузиуса следует, что для равновесного процесса
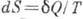 есть полный дифференциал ф-ции состояния S, наз. энтропией. Если учесть первое начало термодинамики, согласно к-рому
есть полный дифференциал ф-ции состояния S, наз. энтропией. Если учесть первое начало термодинамики, согласно к-рому

(U - внутр. энергия, P- давление, V- объём), то из В. н. т. следует, что существует интегрирующий множитель T-1, к-рый делает выражение (2) полным дифференциалом
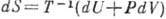 . Поэтому В. и. т. можно сформулировать в виде неравенства
. Поэтому В. и. т. можно сформулировать в виде неравенства 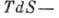
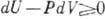 . Неравенство Клаузиуса можно записать в след. виде:
. Неравенство Клаузиуса можно записать в след. виде: 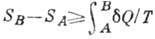 (знак равенства соответствует обратимым процессам). Это неравенство - другая, интегральная формулировка В. н. т. Из него следует, что для адиабатически изолиров. системы
(знак равенства соответствует обратимым процессам). Это неравенство - другая, интегральная формулировка В. н. т. Из него следует, что для адиабатически изолиров. системы 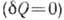 при необратимых процессах энтропия возрастает, а при обратимых - остаётся неизменной.
при необратимых процессах энтропия возрастает, а при обратимых - остаётся неизменной.
Др. эквивалентные формулировки В. н. т. можно получить с помощью любого термодинамического потенциала. Напр., для Гельмгольца энергии (свободной энергии)
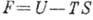 получим
получим 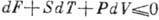 .
.
При выборе в качестве термодинамич. потенциала Гиббса энергии
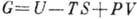 получим
получим 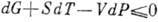
В кинетич. теории газов В. н. т. является следствием Болъцмана Н-теоремы, т. к. Н -функция Больцмана, определяемая через ср. логарифм ф-ции распределения атомов, пропорциональна энтропии идеального газа. Поэтому убывание энтропии имеет не абсолютный, а вероятностный характер.
В статистич. физике выясняется физ. смысл энтропии, связанной с логарифмом термодинамической вероятности W соотношением Больцмана
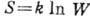 . Термодинамич. вероятность
. Термодинамич. вероятность 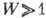 определяется статистич. весом макроскопич. состояния. Возрастание энтропии означает переход системы из менее вероятного состояния в более вероятное.
определяется статистич. весом макроскопич. состояния. Возрастание энтропии означает переход системы из менее вероятного состояния в более вероятное.
В термодинамике неравновесных процессов В. н. т. оказывается следствием положительности производства энтропии (т. е. скорости её возрастания), к-рое является положительно определённой квадратичной формой от термодинамич. сил, характеризующих отклонение системы от состояния термодинамич. равновесия. T. о., неравновесная термодинамика даёт количественную характеристику В. н. т.
В статистич. физике устанавливают пределы применимости В. н. т., связанные с существованием флуктуации энтропии. Вывод о "тепловой смерти" Вселенной, к-рый иногда делают на основе применения к ней В. н. т. как к замкнутой термодинамич. системе, не является правомерным. Ошибочны также попытки опровергнуть этот вывод, учитывая возможность флуктуации, как это было сделано Л. Больцманом (L. Boltzmann). Дело в том, что в эволюции Вселенной существ. роль играет тяготение, к-рое не принималось во внимание.
Лит. см. при ст. Термодинамика. Д. H. Зубарев.
Физическая энциклопедия. В 5-ти томах. — М.: Советская энциклопедия. Главный редактор А. М. Прохоров. 1988.
.
