- ОКСИАНТРАХИНОНЫ
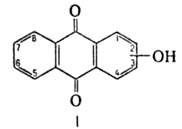
(гидроксиантрахиноны), производные антрахинона, содержащие в молекуле одну или неск. гидроксильных групп. Практич. значение имеют 1- и 2- (ф-ла I), дигидроксиантрахиноны - ализарин и хинизарин, а также мн. полигидроксиантрахиноны. О.-кристаллы от желтого до красного и коричневого цвета (см. табл.); раств. в ледяной СН 3 СООН, этаноле, диэтиловом эфире, пиридине, ароматич. углеводородах, мало или практически не раств. в воде.
СВОЙСТВА НЕКОТОРЫХ ГИДРОКСИАНТРАХИНОНОВ
Положение групп ОН в ядре антрахинона
Тривиальное назв.
Мол. м.
Т. пл., °С
Т. кип., °С
1
Эритроокси-антрахинон
224,2
194-195
Возгоняется
2
-
224,2
306
То же
1,2
Ализарин
240,2
289
430
1,4
Хинизарин
240,2
202
450 (с разл.)
1,5
Антраруфин
240,2
280
Возгоняется
1,8
Хризазин
240,2
193
Разлагается
2,6
Антрафлавин
240,2
>360
Возгоняется
1,2,3
Антрагаллол
256,2
313-4
290 (с возг.)
1,2,4
Пурпурин
256,2
259
Возгоняется
1,2,6
Флавопурпурин
256,2
360
459
1,2,7
Антрапурпурин
256,2
374
462
1,2,5,8
Хинализарин
272,2
313-16
Возгоняется
1,4,5,8
-
272,2
350
То же
1,2,4,5,8
Ализаринцианин R
288,2
-
-"-
1,2,3,5,6,7
Руфигалловая к-та
304,2
-
-
1,2,4,5,6,8
Ализаринцианин WRR
304,2
-
-
Большинство О. и их производных найдены в природе в своб. состоянии или в виде гликозидов в насекомых, грибах, лишайниках, корнях растений; напр., пурпурин, как и ализарин, с древнейших времен извлекают из корней краппа семейства марены красильной (Rubia tinctorum и др. виды), кермес (кермесовая к-та; ф-ла II) и кошениль (карминовая к-та; III)-из неск. видов насекомых (Coccus ilicis и др.) подотряда кокцидовых из группы червецов.

Для 1-О. характерно наличие внутримол. водородной связи между атомом Н гидроксигруппы и атомом О карбонильной группы, что является причиной его более низкой реакц. способности по сравнению с др. О.
1-О. при галогенировании SOCl2 в нитробензоле превращ. в 1-гидрокси-4-хлорантрахинон, а в присут. I2 -в 2,4-ди-хлорантрахинон. При бромировании Вг 2 1-О. образует 2,4-дибром-, а 2-О.-1,3-дибромпроизводное. Нитрование 1-О. приводит к смеси 2- и 4-нитропроизводных. Пром. значение имеет нитрование 1,5- и 1,8-дигидроксиантрахино-нов, приводящее к динитропроизводным - полупродуктам в произ-ве синих дисперсных красителей. Сульфирование 1-О. протекает преим. в положение 2, сульфирование 2-О.-В положение 3; 1,5-дигидроксиантрахинон при 135°С сульфируется до 2,6-дисульфопроизводного. Сульфогруппа в положении 2 в сильнощелочной среде легко может обмениваться на гидроксиметильную группу; в слабощелочной среде преобладает замена группы ОН на атом Н.
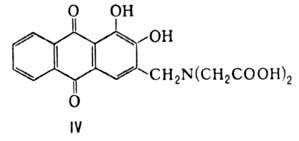
Р-ция ализарина с СН 2 О и иминодиуксусной к-той протекает с образованием ализарин-комплексона ф-лы IV-реагента для фотометрич. определения F, Сu, Са, Ва, Со, Hg, РЗЭ и др. элементов; взаимод. хинизарина с параформом и пиперидином в ДМФА-с образованием 2-пиперидиноме-тил-1,4-дигидроксиантрахинона-промежут. продукта в синтезе катионных красителей.
Пурпурин при нагр. с анилином образует 2-анилино-1,4-дигидроксиантрахинон, к-рый после обработки Н 3 ВО 3 при 160 °С с послед. сульфированием превращ. в протравной краситель для шерсти.
При восстановлении Na2S2O4 в водно-щелочной среде многие О. превращ. в гидроксиантрагидрохиноны (лейко-соединения), обладающие высоким сродством к разл. волокнам и применяемые гл. обр. в кубовом крашении (см. Антрахиноновые красители). Лейкосоединения легко алки-лируются альдегидами, при взаимод. с NH3, аминами и этаноламином замещают гидроксил на группу NH2.
В пром-сти 1-О., 1,5-, 1,8- и 2,6-дигидроксиантрахиноны получают методом известкового плава, нагревая соответствующий сульфонат в автоклаве с суспензией Са(ОН)2, MgCl2 и окислителем (NaNO3, хлорная известь) при 210-230 °С и 2 МПа в течение 10-15 ч.
1-О.-исходный продукт в синтезе замещенных антрахино-нов, 1,8- и 1,4-дигидроксиантрахиноны-промежут. продукты в синтезе разл. фармацевтич. препаратов-антибиотиков антрациклинов, проявляющих противоопухолевую активность, противовоспалит. и слабит. ср-в, а также красителей.
Пурпурин получают окислением ализарина МnО 2 или конденсацией фталевого ангидрида с гидрохиноном с послед. окислением образующегося хинизарина МnО 2; исходное сырье для получения протравного красителя для шерсти. Флавопурпурин и антрапурпурин синтезируют окислит. щелочным плавлением 2,6- и 2,7-антрахинондисульфокислот соотв.; применяют в качестве красителя в ситцепечатании. Антрагаллол (с примесью 1,2,3,5,6,7-гексагидропроизводно-го) получают, нагревая смесь бензойной и 3,4,5-тригид-роксибензойной к-ты с конц. H2SO4 или разб. олеумом; в пром-сти-краситель антраценовый коричневый FF, или ализариновый коричневый для крашения хлопка.
Хинализарин синтезируют обработкой ализарина 70-80%-ным олеумом в присут. Н 3 ВО 3 при 25-30 °С с послед. гидролизом (р-ция Бона-Шмидта); пром. краситель для хлопка, реагент в аналит. химии.
1,2,4,5,6,8-Гексагидроантрахинон-пром. краситель антраценовый синий R, или ализаринцианин WRR, получают при нагр. 1,5-дигидроксиантрахинона с дымящей H2SO4; применяют для окрашивания шерсти в синий цвет по хромовой протраве.
Лит.: Горелик М. В., Химия антрахинонов и их производных, М., 1983.
С. И. Диденко.
Химическая энциклопедия. — М.: Советская энциклопедия. Под ред. И. Л. Кнунянца. 1988.
