- ОКСАДИАЗОЛЫ
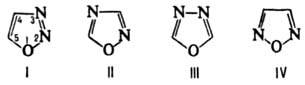
мол. м. 70,06. Различают 1,2,3-, 1,2,4-, 1,3,4- и 1,2,5-О. (ф-лы соотв. I-IV). О.-бесцв. жидкости или кристаллы (см. табл.). Известны замещенные 1,2,3-О., имеющие структуру сид-нонов и сиднониминов (см. Мезоионные соединения).
Незамещенный 1,2,4-О.-неустойчивая жидкость, 3-метил-производное стабильно при 0°С, 5-фенилпроизводное - при 20 °С. 3,5-Дизамещенные производные устойчивы к нагреванию, инертны к действию конц. H2SO4 и дымящей HNO3. Замещенные 1,2,4-О. не вступают в электроф. замещение по атомам С цикла. Нуклеоф. замещение легче всего протекает в положение 5; напр., атом хлора в 5-хлор-3-алкил(арил)-1,2,4-О. легко замещается на амино-, гидрокси- и алкокси-группы.
Под действием к-т, щелочей или восстановителей происходит раскрытие цикла, напр.:
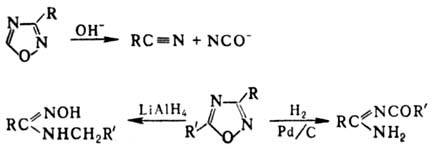
3-Винил- и 5-винил-3-фенил-1,2,4-О. легко полимеризуются; используются для получения синтетич. волокон (см. Термостойкие волокна).
СВОЙСТВА НЕКОТОРЫХ ОКСАДИАЗОЛОВ
Соединение
Мол. м.
Т. пл., °С
Т. кип., °С
1 ,2,4-Оксадиазолы
5-Метил-З-фенил- 1 ,2,4-оксадиазол
160,17
41-42
_
3-Метил-5-фенил-1,2,4-оксадиазол
160,17
55-56
-
3,5- Дифенил-1 ,2,4-оксадиазол
222,25
108
210/17 мм рт. ст.
1 ,3,4-Оксадиазолы
.
1,3,4-Оксадиазол
70,06
_
150-151
2,5-Диметил-1 ,3,4-оксадиазол
98,1
_
178-179
2-Метил-5-фенил- 1 ,3,4-оксадиазол
160,17
61-64
_
2,5- Дифенил-1 ,3,4-оксадиазол
222,25
138-140
231/13 мм рт. ст.
Осн. методы синтеза производных 1,2,4-О.- пиролиз О-ациламидоксимов, конденсация амидоксимов с гидрохлоридами иминоэфиров, р-ции 1,3-диполярного циклоприсое-динения N-оксидов нитрилов с нитрилами:
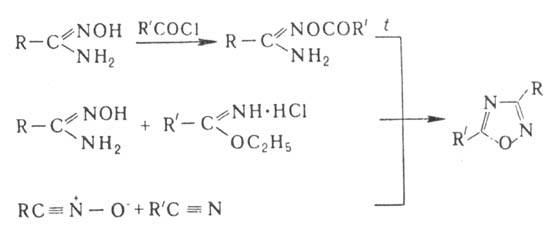
1,3,4-О. и его производные хорошо раств. в большинстве орг. р-рителей (низшие 2-алкил- и 2,5-диалкил-1,3,4-О. раств. в воде); образуют комплексные соед. с AgNO3 и HgCl2; мн. производные 1,3,4-О. обладают высокой термич. стабильностью.
Для 1,3,4-О. и его монозамещенных р-ции электроф. замещения (нитрование, сульфирование) не характерны, галогенирование протекает с трудом; 2,5-диарил-1,3,4-О. с галогенами образуют комплексы. Действие нуклеоф. реагентов на производные 1,3,4-О. обычно приводит к расщеплению цикла или к образованию др. гетероцикла. Аналогично протекает кислотный или щелочной гидролиз:
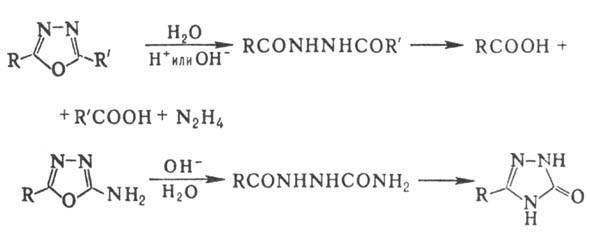
По легкости кислотного гидролиза замещенные 1,3,4-О. располагаются в ряд: 2-алкил-
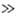 2-арил- > 2-алкокси-5-арил- > > 2,5-диалкил- > 2-алкил-5-арил
2-арил- > 2-алкокси-5-арил- > > 2,5-диалкил- > 2-алкил-5-арил 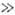 2,5-диарил. 2,5-Диалкил-, 2-алкил-5-арил- и 2,5-диариллроизводные при нагр. с форм-амидом (170-180 °С) или с первичными ариламинами (240-280 °С) образуют производные 1,2,4-триазола:
2,5-диарил. 2,5-Диалкил-, 2-алкил-5-арил- и 2,5-диариллроизводные при нагр. с форм-амидом (170-180 °С) или с первичными ариламинами (240-280 °С) образуют производные 1,2,4-триазола:
Метод получения незамещенного 1,3,4-О. и его 2-замещен-ных - нагревание N-ацилгидразинов с ортомуравьиным эфиром:
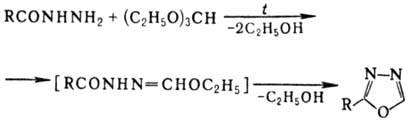
Симметричные 2,5-диалкил-1,3,4-О. получают взаимод. кар-боновых к-т с N2H4
Химическая энциклопедия. — М.: Советская энциклопедия. Под ред. И. Л. Кнунянца. 1988.
