- КЁНИГСА-КНOРРА РЕАКЦИЯ
- получение ацилированных О - алкилгликозидов взаимод. ацилгликозилгалогенидов со спиртами или фенолами, напр.:
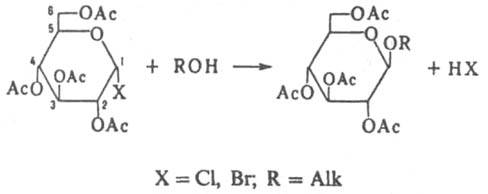
В широком смысле под К.- К. р. понимают аналогичную р-цию гликозилгалогенидов, содержащих разл. образом защищенные гидроксильные группы углеводного остатка. Р-цию проводят в среде спирта - реагента или в инертных р-рителях (СНС13, СН 2 С12, нитрометан, ацетонитрил и др.) при комнатной или несколько повыш. т-ре в присут. катализатора (Ag2O или Ag2CO3) и осушителя (обычно CaSO4). Катализатор одновременно служит акцептором НХ, выделяющегося в р-ции. Р-ция может протекать с участием ацилоксигруппы (путь а)или по механизму SN2 (путь б),напр.:
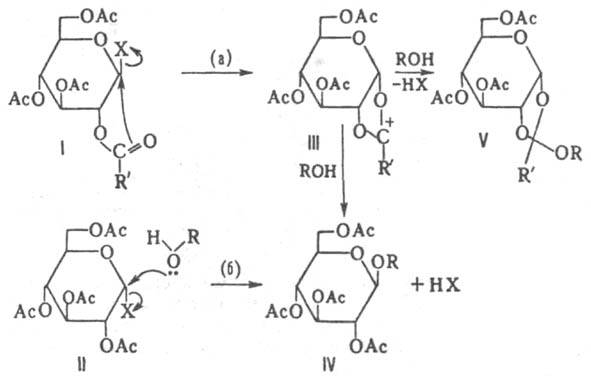
Реализация того или иного пути р-ции, а следовательно, и состав продуктов определяются конфигурацией заместителей у атомов С-1 и С-2 в исходном галогениде, характером группы при С-2, природой акцептора НХ, полярностью среды и др. факторами. По пути (а)К.-К. р. 1,2 - транс- ацилгликозилгалогенидов протекает с участием ацилоксигруппы через промежут. катион (III) с образованием 1,2- транс -ацилгликозида (IV) или ортоэфира (V). С 1,2- цис -ацилгликозилгалогенидами (II) р-ция идет обычно с образованием 1,2- транс -гликозидов (IV), в нек-рых случаях - ортоэфиров. Наличие в исходном соед. (VI) у атома С-2 защитной группы, не участвующей в р-ции по С-1 (напр., бензилоксигруплы), дает возможность получать по К.- К. р. 1,2- цис -гликозиды (VIII); при этом р-ция протекает через образование гликозил-катиона (VII) по механизму SN1, напр.:
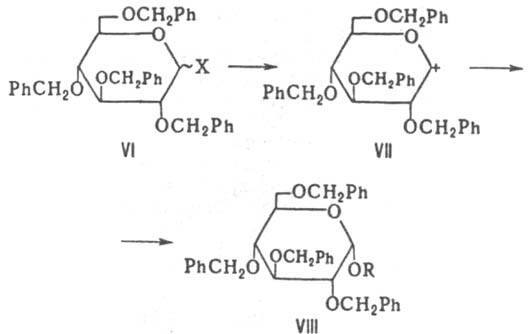
Модификации К.-К. р.: 1) использование в качестве катализатора Hg(COOCH3)2 или Hg(CN)2; р-ция протекает в гомог. среде (модификация Гельфериха). В этих условиях из 1,2- цис -ацилгликозилгалогенидов образуется смесь 1,2- цuc- и 1,2- транс -гликозидов; 2) использование в качестве катализатора смеси HgO и HgBr2 (модификация Шредера). К.- К. р.- один из основных методов синтеза гликозидов и олигосахаридов. В ряду альдоз К.-К. р. носит достаточно общий характер применительно к синтезу пиранозидов (производных моно- и олигосахаридов); синтез фуранозидов по этой р-ции затруднен из-за низкой устойчивости соответствующих галогенидов. Для синтеза гликозидов кетоз (кетозидов) К.-К. р. почти не используется вследствие образования сложной смеси продуктов р-ции. Конденсация, аналогичная К.-К. р., была описана А. Михаэлем в 1879 применительно к синтезу арилгликозидов, В. Кёнигсом и Э. Кнорром в 1901 - для гликозилирования спиртов, а также Э. Фишером и Г. Армстронгом в 1901. Традиционно авторство открытия этой р-вдш приписывают В. Кёнигсу и Э. Кнорру. Лит.. Бочков А. Ф., Афанасьев В. А., Заиков Г Е., Образование и расщепление гликозидных связей. М.. 1978; Igarashi К., "Adv. Garbohydr. Chem. Biochem.", 1977, v. 34, p. 243 83; Восhkоv A. F., Zaikоv G. E., Chemistry of the O-glycosidic bond. Formation and cleavage, Oxf., 1979. А. Ф. Бочков.
Химическая энциклопедия. — М.: Советская энциклопедия. Под ред. И. Л. Кнунянца. 1988.
