- Микрохимия
-
К М. в широком смысле должны были бы быть отнесены вообще все методы химического анализа над веществами в минимальных количествах; но обыкновенно к микрохимическим исследованиям причисляют только те, которые связаны с употреблением микроскопа, так что, например, спектральные исследования или исследования с паяльной трубкой уже не относятся к М. Это сравнительно еще новая область химии. Некоторые микрохимические реакции применялись уже давно ботаниками, физиологами, минералогами, например реакции на крахмал, клетчатку и проч., но эти приемы носили случайный характер, и только в последние 10—20 лет были выработаны общие методы микрохимического анализа, и то лишь для минеральных веществ. Их мы и будем иметь в виду при дальнейшем изложении. Здесь при анализе, при производстве качественных испытаний, например на присутствие той или другой примеси, на полноту осаждения, промывания и проч., знакомство с М. в настоящее время может оказать громадную услугу. Что касается исследования органических веществ, то существуют попытки собрать в одно целое различные единичные наблюдения и систематизировать их; но по своей сложности эта задача является крайне трудной. При выработке методов микрохимического анализа главная задача всех исследователей состояла в том, чтобы найти такие условия при производстве испытаний, при которых можно было бы пользоваться обычными приемами аналитической химии: различием в растворимости, в летучести, прочности, окраске и проч. При этом громадное значение приобрел один из признаков, служащих для характеристики и определения натуры получающихся веществ, а именно внешний вид или их кристаллическая форма — признак, который, как известно, играет ничтожную роль при обычном анализе. Роль этого признака в М. так велика, что в первое время работы этого рода носили скорее кристаллографический характер, чем химический; требовалась большая опытность в пользовании микроскопом и умение разбираться в кристаллографических формах. В настоящее время для определения натуры принимается в расчет только общий вид получающихся при анализе соединений, не касаясь нисколько тонкостей их кристаллического строения. Прежде чем перейти к изложению хода микрохимического анализа, необходимо предварительно ознакомиться: 1) с приборами, употребляющимися здесь, различными манипуляциями, реагентами и проч., словом — техникой исследования, и 2) реакциями и соединениями, характерными для каждого элемента.I. Техника. Микроскоп, годный для обычных микрохимических исследований, должен давать увеличение от 50 до 200 раз. К более сильному увеличению приходится прибегать чрезвычайно редко. Приспособления для нагревания столика микроскопа и для передвижения его при анализе минеральных веществ совершенно излишни. Недурно, конечно, иметь николевы призмы, приспособления для измерения углов кристаллов и разные приспособления для освещения предметов (например, Аббе) и проч., но это не составляет необходимости. Громадное значение имеет при микрохимических работах расстояние объектива от наблюдаемого предмета; чем оно больше, тем микроскоп удобнее, так как это облегчает различные манипуляции, например отделение кристаллов иглой, испытание их твердости, введение реактивов под микроскоп и проч., не боясь испортить при этом чечевицу объектива. Для слабых увеличений это расстояние должно быть 20—30 мм, для больших — не менее 3 мм. Чтобы сделать это расстояние как можно большим, когда приходится прибегать к сильным увеличениям, стараются комбинировать слабый объектив с сильным окуляром. Чем больше поле зрения в микроскопе, тем лучше. Хотя здесь приходится иметь дело с различными едкими веществами (летучие кислоты, щелочи и проч.), но особого ухода и особых предосторожностей при употреблении микроскоп, вообще говоря, не требует; только при работе с фтористо-водородной кислотой или фтористым аммонием необходимо принимать особые меры, чтобы не попортить стекол микроскопа. В этом случае самое удобное смочить объектив каплей воды или глицерина и покрыть его покровным стеклышком или пластинкой слюды. После опыта нужно, конечно, тщательно вымыть и вытереть его. Полезно, если микроскоп снабжен сеточкой для измерения величины кристаллов. При микрохимических исследованиях большинство операций (осаждение, выпаривание и проч.) производится на обыкновенных предметных стеклышках. Они не должны трескаться при резком изменении температуры и легко изменяться от действия реагентов. В тех случаях, когда приходится прибегать к фтористо-водородной кислоте или фтористому аммонию, для предохранения стеклышек покрывают их тонким слоем канадского бальзама, растворенного в скипидаре. Скипидар удаляют осторожным нагреванием. Если нагревать слишком долго или сильно, слой будет с трещинами или бурого цвета; если испарять при обыкновенной температуре, то потребуется очень продолжительное время. Для ускорения этой операции бальзам можно подсушить, а вместо скипидара брать даже эфир или сероуглерод и не упускать из вида, что щелочи разъедают такой слой. В последнее время такого рода стекла заменяют с удобством пластинками из целлулоида. Покровные стекла играют ничтожную роль, так как при исследовании пробы не закрываются. Эти стеклышки служат для возгонки, быстрого нагревания и проч. Для нагревания при высокой температуре, для прокаливания служат небольшие платиновые ложечки. Ложечки с короткой ручкой берутся щипцами с платиновыми наконечниками. Из платиновых вещей необходимы еще шпатели и в особенности платиновые проволочки: они служат для того, чтобы брать капли реактивов, смешивать их под микроскопом и проч. Проволоку около 0,5 мм толщиной нарезают кусочками в 25 мм и впаивают в стеклянные палочки. Платина в листочках употребляется, если нужно на каком-либо минерале известное только место подвергнуть действию реактива. На платиновом листочке делают отверстие, края его сглаживают и приклеивают канадским бальзамом к минералу так, чтобы отверстие приходилось против желаемого места; потом удаляют отсюда бальзам спиртом, тогда реактив действует только на это место. Чтобы брать реактивы по каплям, пользуются проволочками или пипетками из капиллярных стеклянных трубок. Для отделения жидкости от осадка и промывания существует несколько приемов. Прежде всего стараются, чтобы осадок вполне осел. Чтобы ускорить оседание, если жидкости сравнительно много, например более 0,2 куб. стм, прибегают к центрифугированию (2000—3000 оборотов в минуту). Жидкость помещается в тоненькие трубочки с оттянутыми кончиками, на которые надевают каучуковые шапочки; верхнее отверстие закрывают бумагой. Достаточно 2—5 минут центрифугирования, чтобы наиболее трудно отстаиваемые осадки осели. После оседания жидкость удаляют пипеткой, осадок взбалтывают с водой и снова подвергают центрифугированию. Осадок скопляется в оттянутой части трубочки; его при нагревании вытряхивают на стеклянную пластинку. Иногда, чтобы облегчить оседание, к жидкости прибавляют какого-нибудь нерастворимого вещества, например сернокислого бария, хлористого серебра и проч. Когда жидкости немного, например одна капля, то, дав жидкости немного отстояться, стеклянную пластинку, где она находится, понемногу наклоняют и стараются постепенно проволочкой перевести прозрачную жидкость на другое место, где она снова собирается в каплю. Когда это достигнуто, если между каплями существует соединение, его уничтожают, пластинку ставят снова горизонтально, к осадку прибавляют каплю воды, и поступают по-прежнему. Иногда удобно бывает предварительно выпарить жидкость с осадком и потом обработать его соответственным растворителем. Иногда жидкость приходится фильтровать: пластинку с каплей помещают на коробочку или деревянную подставку, несколько скошенную так, что пластинка наклонена вперед. Передний конец ее выдвигают на несколько мм за край подставки; под ним кладут другое стекло. Потом вырезают из пропускной бумаги полоску вида Y (1 мм ширины и 10 мм длины), смачивают ее водой и прикрепляют верхние концы ее к верхней пластинке, а нижний к нижней. После этого заставляют жидкость стечь к бумаге, по которой она и станет фильтроваться вниз. Этим путем нельзя профильтровать менее 0,01 куб. стм жидкости и может быть некоторая потеря осадка. Если жидкость не нужна, можно прямо удалить ее бумагой или необожженной известью.Реактивы. При микрохимическом исследовании одни из реагентов применяются в твердом виде, другие в растворе; но их берут в таком ничтожном количестве, что весь набор реактивов с различными мелкими предметами, необходимыми для анализа, занимает объем не более 1000 куб. стм. Реактивы сохраняют в стеклянных, очень маленьких склянках с притертыми или обыкновенными пробками. Наиболее употребительны: 1) Вода: она должна чаще возобновляться, так как при хранении растворяет стекло; 2) спирт; 3) серная кислота, разбавленная равным объемом воды; 4) азотная кислота удельного веса 1,4, разбавленная объемом воды; 5) соляная кислота удельного веса 1,12; 6) фтористо-водородная кислота; 7) фтористый аммоний; 8) уксусная кислота, разбавленная 1/10 частью воды; 9) муравьиная кислота; 10) щавелевая кислота в мелких кристаллах или порошке; 11) винная кислота, измельченная; 12) кремнекислота в порошке; 13) едкое кали в порошке; 14) едкий натр; 15) аммиак удельного веса 0,93; 16) магний в порошке; 17) цинк в листочках; 18) железо в проволоке; 19) олово; 20) калийная селитра; 21) бертолетова соль; 22) перекись водорода; 23) азотисто-калиевая соль, насыщенный раствор; 24) сода в порошке; 25) углекислый аммоний; 26) хлористый рубидий; 27) хлористый цезий; 28) хлористый натрий; 29) хлористый аммоний; 30) йодистый калий; 31) желтая соль; 32) роданистый аммоний, насыщенный раствор; 33) кремнефтористо-водородный аммоний; 34) серно-калиевая соль; 35) серно-натриевая соль; 36) двухромокалиевая соль; 37) щавелевокислый калий, кислая и средняя соли; 38) сегнетова соль; 39) уксусно-натровая соль; 40) фосфорно-натровая соль; 41) молибденовокислый аммоний; 42) азотнокислый таллий; 43) уксуснокислый барий; 44) уксуснокислый стронций; 45) у. кальций; 46) у. магний, насыщенный раствор, 47) у. цинк; 48) у. свинец; 49) у. медь; 50) у. кобальт; 51) у. уран; 52) азотнокислый висмут; 53) азотнокислое серебро; 54) сулема; 55) хлорное олово, концентрированный раствор; 56) хлорная платина, раствор 1:10; 57) хлороплатинат калия, насыщенный раствор; 58) сернокислая платина, раствор 1:20; 59) крахмал; 60) лакмус в растворе; 61) краски Congoroth и Malachit-grün и некоторые другие реактивы. Все эти вещества должны быть совершенно чисты, в чем необходимо убедиться соответственными испытаниями.Характерные реакции. Микрохимический анализ минеральных веществ настолько разработан, что для каждого элемента найдены соединения, более или менее для него характерные. В выборе этих характерных соединений главным образом руководствовались следующим принципом: иметь соединения сравнительно малорастворимые и выделяющиеся по возможности в больших, хорошо образованных кристаллах. Соединения, выделяющиеся в аморфном виде или в очень мелких (под микроскопом) кристаллах, не относятся к характерным, хотя бы растворимость их была значительно ниже. Реакции цветные вообще не играют здесь почти никакой роли. Что касается таких реакций, которые служили бы для отделения одной группы элементов от другой, как при обычном анализе, то здесь об этом нет и речи. Микрохимический анализ является только подспорьем при аналитических работах, чтобы убедиться в присутствии того или другого элемента; на систематический ход анализа, когда предполагается одновременное присутствие всех элементов, здесь не рассчитывают. Для удобства при описании соединений, характерных для различных элементов, мы будем располагать последние в том порядке, в котором они находятся в курсах аналитической химии, т. е. сначала металлы 1, 2, 3, 4 и 5 группы, а затем металлоиды, останавливаясь притом только на более распространенных элементах.Калий определяется в виде хлороплатината K2PtCl6, фосфоромолибдата K3РО4.10МоО3+3H2O и двойной сернокислой соли с висмутом 3K2SO4.Bi2(SO4)3. 1) K2PtCl6 получается из нейтральных или слабокислых растворов солей калия при действии хлорной платины. Концентрированные растворы дают сразу массу мелких октаэдров, разбавленные при медленном испарении выделяют очень хорошо образованные октаэдры лимонно-желтого цвета и комбинации октаэдра с кубом (фиг. 1).
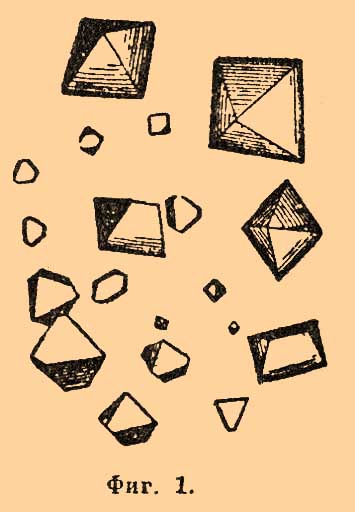 Фиг. 1.Крепкие кислоты растворяют K2PtCl6; их нейтрализуют частью содой, частью уксусно-натриевой или уксусно-магнезиальной солью; спирт уменьшает растворимость. Это одна из характернейших реакций на калий при отсутствии аммония, рубидия и цезия. 2) Фосфорно-молибденовая соль калия выделяется при действии фосфорно-молибденовой кислоты на подкисленный азотной кислотой раствор калийной соли; хорошие кристаллы похожи на K2PtCl6, обыкновенно же получаются сферические зерна. Реакция характерна при отсутствии NH3, Rb, Cs. 3) Для получения 3K2SO4.Bi2SO4)3 растворяют немного азотнокислого висмута в капле серной кислоты и действуют этим раствором на сильно концентрированный раствор калийной соли (даже можно прямо на твердую соль); образуются шестиугольные бесцветные таблички. Для характеристики калия служит также кремнефтористо-водородная соль K2SiF6, хлорно-калиевая.Натрий характеризуется образованием двойной соли с уксуснокислым ураном, соединением с уксуснокислым ураном и магнием, в виде кремнефтористо-водородной соли. 1) Для получения двойной уксусно-урановой соли NaC2H3O2UO2(C2H3O2)2 растворяют уксуснокислый уран лучше всего в разбавленной уксусной кислоте и действуют им на очень сгущенный раствор натровой соли; появляются бесцветные тетраэдры или комбинация двух тетраэдров (фиг. 2).
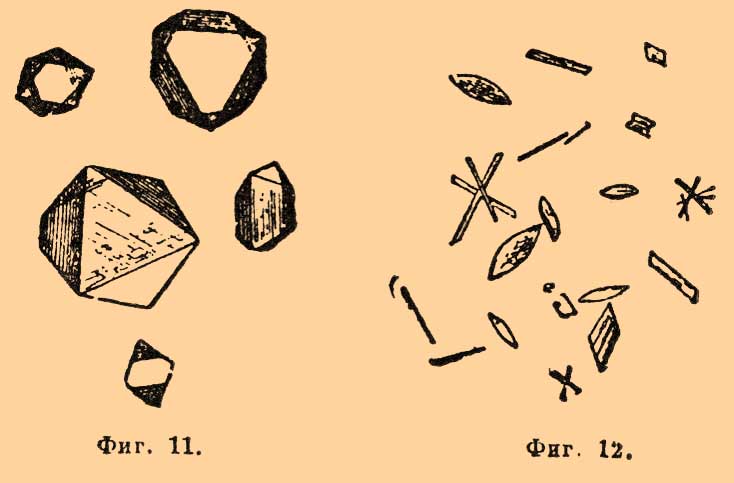
Фиг. 1.Крепкие кислоты растворяют K2PtCl6; их нейтрализуют частью содой, частью уксусно-натриевой или уксусно-магнезиальной солью; спирт уменьшает растворимость. Это одна из характернейших реакций на калий при отсутствии аммония, рубидия и цезия. 2) Фосфорно-молибденовая соль калия выделяется при действии фосфорно-молибденовой кислоты на подкисленный азотной кислотой раствор калийной соли; хорошие кристаллы похожи на K2PtCl6, обыкновенно же получаются сферические зерна. Реакция характерна при отсутствии NH3, Rb, Cs. 3) Для получения 3K2SO4.Bi2SO4)3 растворяют немного азотнокислого висмута в капле серной кислоты и действуют этим раствором на сильно концентрированный раствор калийной соли (даже можно прямо на твердую соль); образуются шестиугольные бесцветные таблички. Для характеристики калия служит также кремнефтористо-водородная соль K2SiF6, хлорно-калиевая.Натрий характеризуется образованием двойной соли с уксуснокислым ураном, соединением с уксуснокислым ураном и магнием, в виде кремнефтористо-водородной соли. 1) Для получения двойной уксусно-урановой соли NaC2H3O2UO2(C2H3O2)2 растворяют уксуснокислый уран лучше всего в разбавленной уксусной кислоте и действуют им на очень сгущенный раствор натровой соли; появляются бесцветные тетраэдры или комбинация двух тетраэдров (фиг. 2).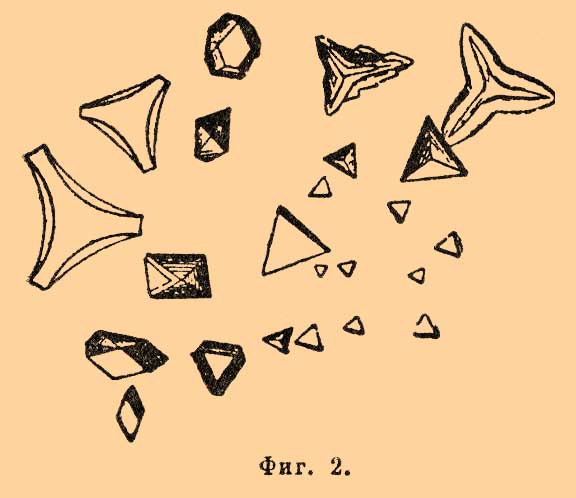 Фиг. 2.Крепкие кислоты, а также присутствие аммиачных солей и хлорной платины вредят ясности этой реакции. 2) Тройная уксуснокислая соль натрия, магния и урана образуется в тех же условиях в присутствии магнезиальных солей из слабых растворов натриевых солей (из крепких образуется предыдущая соль); большие кристаллы ромбической системы, с виду напоминающие тетраэдры. Такие же соединения получаются с солями железа, кобальта, никеля, меди, цинка, кадмия и бериллия. 3) Na2SiF6 получается при действии крепкого раствора или твердого кремнефтористого аммония. Из крепких растворов натровых солей выделяются шестиугольные звездочки, из слабых — таблички слабо-розового цвета (фиг. 3). Присутствие аммиачных солей и хлорной платины здесь не играет никакой роли. В нейтральных или щелочных растворах характерно для натрия образование призматических кристаллов пиросурьмяно-натриевой соли (при отсутствии кальция и магния). Слабые растворы этой соли при испарении легко становятся пересыщенными, и кристаллизация вызывается растиранием проволочкой и прибавлением спирта.Аммоний — см. дальше азот.Литий характеризуется образованием фтористого лития LiF, фосфорнокислого Li3PO4 и углекислого лития Li2CO3. 1) LiF выделяется в виде кубов. 2) Li3PO4 требует нагревания для своего образования. Из нейтральных растворов при действии фосфорно-натриевой соли она выделяется в виде четырехугольных табличек, палочек и проч. 3) Li2CO3 выделяется из слабых растворов при действии углекислого аммония в виде тонких иголочек, напоминающих гипс.Цезий характеризуется двойной солью с хлорным оловом Cs2SnCl6 (бесцветные октаэдры; фиг. 4), силикомолибдатом, при действии кремнемолибденового аммония на раствор соли Cs, и хлороплатинатом Cs2PtCl6. Наиболее характерно для Cs образование Cs2PtCl6; для получения его берут очень слабый раствор PtCl4 (1:200) или насыщенный раствор K2PtCl6; октаэдры слабо-желтого цвета.Рубидий характеризуется образованием: 1) хлороплатината Rb2PtCl6 и 2) силикомолибдата. Они схожи с соответственными соединениями цезия.Магний определяется в виде фосфорно-аммиачно-магнезиальной соли NH4MgPO4+6H2O и пиросурьмяной. 1) Для получения NH4MgPO4+6H2O к пробе прибавляют хлористого аммония и аммиака, нагревают и действуют фосфорно-натриевой солью; из крепких растворов выделяются крестообразные кристаллы, из очень слабых — неправильные призмы (фиг. 5). Это чрезвычайно чувствительная реакция. 2) Пиросурьмяно-магнезиальная соль MgH2Sb2O7+9H2O выделяется из нейтральных растворов в виде шестиугольных призм.Фиг. 3. Фиг. 4. Фиг. 5. Фиг. 6. Фиг. 7. Фиг. 8.Барий характеризуется в виде сернокислой соли BaSO4, кремнефтористо-водородной соли BaSiF6, хромовокислой соли BaCrO4 и в виде двойной виннокислой соли бария и сурьмы Ba(SbOC4H4O6)2+2H2O. 1) BaSO4 выделяется в виде аморфных зерен. Нерастворимость его в воде и соляной кислоте отличают его от сернокислого кальция и стронция. BaSO4 растворяется в крепкой серной кислоте при нагревании и выделяется при охлаждении в виде звездочек (фиг. 6). 2) BaSiF6 выделяется в виде иголочек и звездочек (фиг. 7). Азотная и соляная кислоты вредят чувствительности, уксусная кислота — без влияния. Стронций и кальций не показывают этой реакции. 3) BaCrO4 получается при нагревании, при действии Ka2Cr2O7 на раствор соли бария, к которой прибавлено уксусно-натриевой соли и уксусной кислоты; четырехугольные таблички. Уксусная кислота необходима для того, чтобы затруднить образование SrCrO4, если присутствует стронций. 4) Для получения Ba(SbOC4H4O6)+2H2O к нейтральному или подкисленному уксусной кислотой раствору прибавляют при нагревании соответственной калийной соли; неправильные шестиугольные таблички. В присутствии Sr реакция неприменима, так как последний тоже осаждается. Ca, Mg и щелочи тоже вредят чувствительности. Из других соединений бария характерны углекислая соль ВаСО3 (в виде зерен) и щавелевокислая (палочки).Стронций определяется в виде сернокислой соли SrSO4, хромовокислой SrCrO4, двойной сурьмяно-виннокислой Sr(SbOC4H4O6)2+2H2O и углекислой SrCO3. 1) SrSO4 при кристаллизации из нагретой серной кислоты дает ромбические кристаллы, отличающиеся от BaSO4 (фиг. 8); кроме того, при нагревании они значительно растворяются в соляной кислоте. 2) SrCrO4 осаждается (в виде призм или крупинок) из нейтрального раствора при помощи K2CrO4; уксусная кислота сильно затрудняет образование ее. 3) Sr(SbOC4H4O6)2+2H2O и SrCO3 сходны с соответствующими солями бария. Щавелевокислый стронций осаждается при помощи щавелевой кислоты даже в присутствии некоторого количества азотной кислоты, в виде октаэдров или призм, смотря по условиям.Кальций характеризуется образованием сернокислой соли CaSO4+2Н2O, виннокислой CaC4H4O6+4H2O и двойной калийной железисто-синеродистой K2CaFe(CN)6, а также углекислой. 1) Наиболее характерной реакцией служит образование гипса CaSO4+2Н2O. Из слабых растворов при испарении (при прибавлении спирта из очень слабых) выделяются очень характерные призматические кристаллы (фиг. 9).Фиг. 9.Крепкие кислоты, борная кислота, хлористые соединения алюминия, железа, большое количество щелочных солей вредят чувствительности реакции. Из крепкой серной кислоты выделяются таблички безводного гипса. 2) Виннокислый кальций образуется в растворах нейтральных или подкисленных уксусной кислотой, в виде ромбических призм (фиг. 10); из слабых растворов осаждение идет очень медленно; спирт и нагревание помогают.
Фиг. 2.Крепкие кислоты, а также присутствие аммиачных солей и хлорной платины вредят ясности этой реакции. 2) Тройная уксуснокислая соль натрия, магния и урана образуется в тех же условиях в присутствии магнезиальных солей из слабых растворов натриевых солей (из крепких образуется предыдущая соль); большие кристаллы ромбической системы, с виду напоминающие тетраэдры. Такие же соединения получаются с солями железа, кобальта, никеля, меди, цинка, кадмия и бериллия. 3) Na2SiF6 получается при действии крепкого раствора или твердого кремнефтористого аммония. Из крепких растворов натровых солей выделяются шестиугольные звездочки, из слабых — таблички слабо-розового цвета (фиг. 3). Присутствие аммиачных солей и хлорной платины здесь не играет никакой роли. В нейтральных или щелочных растворах характерно для натрия образование призматических кристаллов пиросурьмяно-натриевой соли (при отсутствии кальция и магния). Слабые растворы этой соли при испарении легко становятся пересыщенными, и кристаллизация вызывается растиранием проволочкой и прибавлением спирта.Аммоний — см. дальше азот.Литий характеризуется образованием фтористого лития LiF, фосфорнокислого Li3PO4 и углекислого лития Li2CO3. 1) LiF выделяется в виде кубов. 2) Li3PO4 требует нагревания для своего образования. Из нейтральных растворов при действии фосфорно-натриевой соли она выделяется в виде четырехугольных табличек, палочек и проч. 3) Li2CO3 выделяется из слабых растворов при действии углекислого аммония в виде тонких иголочек, напоминающих гипс.Цезий характеризуется двойной солью с хлорным оловом Cs2SnCl6 (бесцветные октаэдры; фиг. 4), силикомолибдатом, при действии кремнемолибденового аммония на раствор соли Cs, и хлороплатинатом Cs2PtCl6. Наиболее характерно для Cs образование Cs2PtCl6; для получения его берут очень слабый раствор PtCl4 (1:200) или насыщенный раствор K2PtCl6; октаэдры слабо-желтого цвета.Рубидий характеризуется образованием: 1) хлороплатината Rb2PtCl6 и 2) силикомолибдата. Они схожи с соответственными соединениями цезия.Магний определяется в виде фосфорно-аммиачно-магнезиальной соли NH4MgPO4+6H2O и пиросурьмяной. 1) Для получения NH4MgPO4+6H2O к пробе прибавляют хлористого аммония и аммиака, нагревают и действуют фосфорно-натриевой солью; из крепких растворов выделяются крестообразные кристаллы, из очень слабых — неправильные призмы (фиг. 5). Это чрезвычайно чувствительная реакция. 2) Пиросурьмяно-магнезиальная соль MgH2Sb2O7+9H2O выделяется из нейтральных растворов в виде шестиугольных призм.Фиг. 3. Фиг. 4. Фиг. 5. Фиг. 6. Фиг. 7. Фиг. 8.Барий характеризуется в виде сернокислой соли BaSO4, кремнефтористо-водородной соли BaSiF6, хромовокислой соли BaCrO4 и в виде двойной виннокислой соли бария и сурьмы Ba(SbOC4H4O6)2+2H2O. 1) BaSO4 выделяется в виде аморфных зерен. Нерастворимость его в воде и соляной кислоте отличают его от сернокислого кальция и стронция. BaSO4 растворяется в крепкой серной кислоте при нагревании и выделяется при охлаждении в виде звездочек (фиг. 6). 2) BaSiF6 выделяется в виде иголочек и звездочек (фиг. 7). Азотная и соляная кислоты вредят чувствительности, уксусная кислота — без влияния. Стронций и кальций не показывают этой реакции. 3) BaCrO4 получается при нагревании, при действии Ka2Cr2O7 на раствор соли бария, к которой прибавлено уксусно-натриевой соли и уксусной кислоты; четырехугольные таблички. Уксусная кислота необходима для того, чтобы затруднить образование SrCrO4, если присутствует стронций. 4) Для получения Ba(SbOC4H4O6)+2H2O к нейтральному или подкисленному уксусной кислотой раствору прибавляют при нагревании соответственной калийной соли; неправильные шестиугольные таблички. В присутствии Sr реакция неприменима, так как последний тоже осаждается. Ca, Mg и щелочи тоже вредят чувствительности. Из других соединений бария характерны углекислая соль ВаСО3 (в виде зерен) и щавелевокислая (палочки).Стронций определяется в виде сернокислой соли SrSO4, хромовокислой SrCrO4, двойной сурьмяно-виннокислой Sr(SbOC4H4O6)2+2H2O и углекислой SrCO3. 1) SrSO4 при кристаллизации из нагретой серной кислоты дает ромбические кристаллы, отличающиеся от BaSO4 (фиг. 8); кроме того, при нагревании они значительно растворяются в соляной кислоте. 2) SrCrO4 осаждается (в виде призм или крупинок) из нейтрального раствора при помощи K2CrO4; уксусная кислота сильно затрудняет образование ее. 3) Sr(SbOC4H4O6)2+2H2O и SrCO3 сходны с соответствующими солями бария. Щавелевокислый стронций осаждается при помощи щавелевой кислоты даже в присутствии некоторого количества азотной кислоты, в виде октаэдров или призм, смотря по условиям.Кальций характеризуется образованием сернокислой соли CaSO4+2Н2O, виннокислой CaC4H4O6+4H2O и двойной калийной железисто-синеродистой K2CaFe(CN)6, а также углекислой. 1) Наиболее характерной реакцией служит образование гипса CaSO4+2Н2O. Из слабых растворов при испарении (при прибавлении спирта из очень слабых) выделяются очень характерные призматические кристаллы (фиг. 9).Фиг. 9.Крепкие кислоты, борная кислота, хлористые соединения алюминия, железа, большое количество щелочных солей вредят чувствительности реакции. Из крепкой серной кислоты выделяются таблички безводного гипса. 2) Виннокислый кальций образуется в растворах нейтральных или подкисленных уксусной кислотой, в виде ромбических призм (фиг. 10); из слабых растворов осаждение идет очень медленно; спирт и нагревание помогают.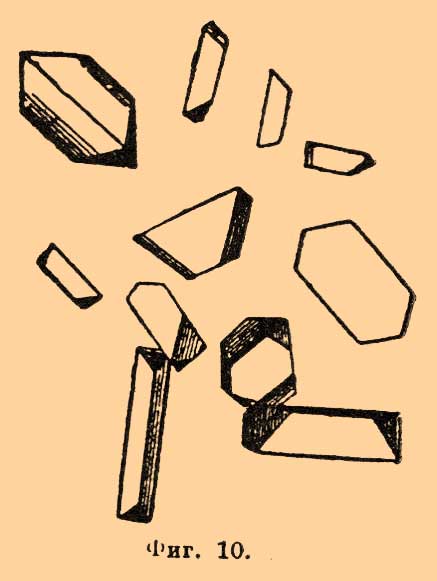 Фиг. 10.В присутствии солей Ba, Sr, Mg, хлористых соединений Al и Fe и борной кислоты чувствительность реакции ослабевает. 3) Железисто-синеродистый калий в избытке осаждает даже из очень слабых растворов четырехугольные таблички K2CaFe(CN)6, в особенности в присутствии NH4Cl. При достаточном разбавлении соли Sr и Ba не дают в этом случае осадка. Щавелевокислый и углекислый кальций являются в очень мелких кристаллах; один в виде четырехгранных пирамид, другой в виде ромбоэдров или иголочек арагонита.Алюминий характеризуется цезиевыми квасцами Cs2SO4.Al2(SO4)3+24H2O и двойной фтористо-водородно-аммиачной солью (NH4)3AlF6. 1) Для получения Cs2SO4Al2(SO4)3+24H2O пробу выпаривают с серной кислотой, разбавляют водой и кладут в нее кристаллик хлористого или сернокислого цезия; выделяются октаэдры и комбинация куба с октаэдром (фиг. 11).Фиг. 11. Фиг. 12.Для получения хороших кристаллов лучше иметь слабые растворы алюминиевой соли и после прибавления CsCl давать жидкости медленно испаряться на воздухе или в эксикаторе. Большое количество щелочных солей вредит чувствительности реакции. В случае надобности из таких растворов выделяют аммиаком водную окись алюминия или основную уксуснокислую соль, промывают, растворяют в HCl и затем проделывают описанную реакцию. Железные соли не вредят реакции. 2) (NH4)3AlF6 образует октаэдры; в присутствии железа реакция неприменима.Железо характеризуется образованием берлинской лазури и двойной соли (NH4)3FeF6. 1) Берлинская лазурь является в виде хлопьев. Нужно избегать присутствия сильных кислот, которые могут вызвать образование лазури из самого реактива. 2) NH4F выделяет с солями железа октаэдры двойной соли (NH4)3FeF6; от соответственной соли алюминия они отличаются тем, что с аммиаком буреют.Хром определяется в виде двухромовокислого серебра Ag2Cr2O7 и хромовокислого свинца; в том и другом случае прежде всего стараются получить хром в виде соединений хромовой кислоты. Когда требуется окисление хромовых соединений, его производят обычным путем (сплавляя с Na2CO3 и NaNO3, кипячением с HNO3 и KClO3 или с помощью перекиси водорода). 1) Раствор хромовой соли подкисляют азотной кислотой и действуют азотнокислым серебром; получаются темно-красные призматические кристаллы, растворимые в NH3 и HNO3. В присутствии большого избытка HNO3 или сернокислых солей образуются ромбические кристаллы Ag2CrO4. Галоиды вредят реакции. 2) При обыкновенной температуре уксуснокислый свинец дает с солями хромовой кислоты мелкий аморфный осадок PbCrO4; в присутствии же большого количества азотной кислоты и при нагревании выделяются желтые палочки и чечевички (фиг. 12).Марганец (в солях марганца) определяется в виде щавелевокислой соли MnC2O4+3H2O, двойной фосфорно-аммиачной NH4MnPO4+6H2O и в виде перекиси MnO2. 1) Щавелевокислый марганец образует очень характерные кристаллы. Присутствие цинка, никеля и кобальта, также калия и натрия и крепких кислот вредит их образованию. В присутствии щавелевокислого аммония выделяются более мелкие звездочки (фиг. 13). 2) Для получения NH4MnPO4+6H2O поступают так же, как описано при Mg, с той разницей, что фосфорно-натриевую соль растворяют в NH3 и реагируют этим раствором. Это делается во избежание окисления аммиачных растворов марганца. Кристаллы, такие же как и для Mg, отличаются от NH4MgPO4 тем, что они, промытые в присутствии KHO и Н2O2, сильно темнеют, сохраняя свою форму. 3) Для получения перекиси MnO2 к аммиачному раствору прибавляют Н2O2; эта реакция служит для отделения Mn от Zn, Mg, Ni; для отделения от Co соединения марганца окисляют азотной кислотой с бертолетовой солью.Фиг. 13. Фиг. 14. Фиг. 16.Цинк определяется в виде двойной углекислой соли с натрием, в виде щавелевокислого цинка, двойной роданистой соли с ртутью и железосинеродистого цинка. 1) Раствор цинковой соли в присутствии аммиачных солей и аммиака выделяет с NaHCO3 мелкие тетраэдры двойной соли 3Na2CO3+8ZnCO3+8H2O (фиг. 14); в этих условиях Cd и Ni дают зернистый осадок, Co — хлопьевидный; реакции вредит Mg. В присутствии большого количества Mg производят разделение — выделяют Zn магнием в металлическом виде или пользуются растворимостью окиси цинка в KHO. 2) Щавелевая кислота выделяет призматические кристаллы ZnC2O4+2Н2O. Магний и кадмий вредят реакции. 3) Раствор роданистой ртути в роданистом аммонии дает ромбические кристаллы Zn(CNS)2.Hg(CNS)2. 4) Железосинеродистый калий дает очень мелкие кубические кристаллы Zn3Fe2(CN)12. Характерны также фосфорнокислая и хромовокислая соли.Кобальт характеризуется образованием двойной азотистокислой соли с калием, двойной роданистой соли со ртутью, двойной фосфорно-аммиачной соли и хлоропурпуреокобальтиака. 1) Двойная азотисто-кобальто-калиевая соль получается из растворов, подкисленных уксусной кислотой в виде желтых зернышек или очень мелких октаэдров или кубов (фиг. 15).
Фиг. 10.В присутствии солей Ba, Sr, Mg, хлористых соединений Al и Fe и борной кислоты чувствительность реакции ослабевает. 3) Железисто-синеродистый калий в избытке осаждает даже из очень слабых растворов четырехугольные таблички K2CaFe(CN)6, в особенности в присутствии NH4Cl. При достаточном разбавлении соли Sr и Ba не дают в этом случае осадка. Щавелевокислый и углекислый кальций являются в очень мелких кристаллах; один в виде четырехгранных пирамид, другой в виде ромбоэдров или иголочек арагонита.Алюминий характеризуется цезиевыми квасцами Cs2SO4.Al2(SO4)3+24H2O и двойной фтористо-водородно-аммиачной солью (NH4)3AlF6. 1) Для получения Cs2SO4Al2(SO4)3+24H2O пробу выпаривают с серной кислотой, разбавляют водой и кладут в нее кристаллик хлористого или сернокислого цезия; выделяются октаэдры и комбинация куба с октаэдром (фиг. 11).Фиг. 11. Фиг. 12.Для получения хороших кристаллов лучше иметь слабые растворы алюминиевой соли и после прибавления CsCl давать жидкости медленно испаряться на воздухе или в эксикаторе. Большое количество щелочных солей вредит чувствительности реакции. В случае надобности из таких растворов выделяют аммиаком водную окись алюминия или основную уксуснокислую соль, промывают, растворяют в HCl и затем проделывают описанную реакцию. Железные соли не вредят реакции. 2) (NH4)3AlF6 образует октаэдры; в присутствии железа реакция неприменима.Железо характеризуется образованием берлинской лазури и двойной соли (NH4)3FeF6. 1) Берлинская лазурь является в виде хлопьев. Нужно избегать присутствия сильных кислот, которые могут вызвать образование лазури из самого реактива. 2) NH4F выделяет с солями железа октаэдры двойной соли (NH4)3FeF6; от соответственной соли алюминия они отличаются тем, что с аммиаком буреют.Хром определяется в виде двухромовокислого серебра Ag2Cr2O7 и хромовокислого свинца; в том и другом случае прежде всего стараются получить хром в виде соединений хромовой кислоты. Когда требуется окисление хромовых соединений, его производят обычным путем (сплавляя с Na2CO3 и NaNO3, кипячением с HNO3 и KClO3 или с помощью перекиси водорода). 1) Раствор хромовой соли подкисляют азотной кислотой и действуют азотнокислым серебром; получаются темно-красные призматические кристаллы, растворимые в NH3 и HNO3. В присутствии большого избытка HNO3 или сернокислых солей образуются ромбические кристаллы Ag2CrO4. Галоиды вредят реакции. 2) При обыкновенной температуре уксуснокислый свинец дает с солями хромовой кислоты мелкий аморфный осадок PbCrO4; в присутствии же большого количества азотной кислоты и при нагревании выделяются желтые палочки и чечевички (фиг. 12).Марганец (в солях марганца) определяется в виде щавелевокислой соли MnC2O4+3H2O, двойной фосфорно-аммиачной NH4MnPO4+6H2O и в виде перекиси MnO2. 1) Щавелевокислый марганец образует очень характерные кристаллы. Присутствие цинка, никеля и кобальта, также калия и натрия и крепких кислот вредит их образованию. В присутствии щавелевокислого аммония выделяются более мелкие звездочки (фиг. 13). 2) Для получения NH4MnPO4+6H2O поступают так же, как описано при Mg, с той разницей, что фосфорно-натриевую соль растворяют в NH3 и реагируют этим раствором. Это делается во избежание окисления аммиачных растворов марганца. Кристаллы, такие же как и для Mg, отличаются от NH4MgPO4 тем, что они, промытые в присутствии KHO и Н2O2, сильно темнеют, сохраняя свою форму. 3) Для получения перекиси MnO2 к аммиачному раствору прибавляют Н2O2; эта реакция служит для отделения Mn от Zn, Mg, Ni; для отделения от Co соединения марганца окисляют азотной кислотой с бертолетовой солью.Фиг. 13. Фиг. 14. Фиг. 16.Цинк определяется в виде двойной углекислой соли с натрием, в виде щавелевокислого цинка, двойной роданистой соли с ртутью и железосинеродистого цинка. 1) Раствор цинковой соли в присутствии аммиачных солей и аммиака выделяет с NaHCO3 мелкие тетраэдры двойной соли 3Na2CO3+8ZnCO3+8H2O (фиг. 14); в этих условиях Cd и Ni дают зернистый осадок, Co — хлопьевидный; реакции вредит Mg. В присутствии большого количества Mg производят разделение — выделяют Zn магнием в металлическом виде или пользуются растворимостью окиси цинка в KHO. 2) Щавелевая кислота выделяет призматические кристаллы ZnC2O4+2Н2O. Магний и кадмий вредят реакции. 3) Раствор роданистой ртути в роданистом аммонии дает ромбические кристаллы Zn(CNS)2.Hg(CNS)2. 4) Железосинеродистый калий дает очень мелкие кубические кристаллы Zn3Fe2(CN)12. Характерны также фосфорнокислая и хромовокислая соли.Кобальт характеризуется образованием двойной азотистокислой соли с калием, двойной роданистой соли со ртутью, двойной фосфорно-аммиачной соли и хлоропурпуреокобальтиака. 1) Двойная азотисто-кобальто-калиевая соль получается из растворов, подкисленных уксусной кислотой в виде желтых зернышек или очень мелких октаэдров или кубов (фиг. 15). Фиг. 15.2) Очень характерна для Co двойная соль Co(CNS)2.Hg(CNS)2 — кристаллы синего цвета; в присутствии Zn и Cd выделяются смеси солей того же вида, слабо окрашенные в синий цвет (фиг. 16). 3) NH4CoPO4 получается так же, как для Mg; от KHO и Н2O2 окрашивается в темный цвет.Никель характеризуется тройной азотистокислой солью калия, никеля и свинца, двойной фосфорно-аммиачно-никелевой солью и щавелевокислой солью. 1) Растворы никелевых солей, подкисленные уксусной кислотой, с KNO2 и уксуснокислым свинцом дают желтые кристаллы K2NiPb(NO2)6, схожие с кристаллами азотисто-кобальто-калиевой соли. Pb может быть заменен Ba, Ca, Sr. 2) Кристаллы NH4NiPO4+2Н2О образуются в тех же условиях, как и для магния (однако, лучше брать углеаммиачную соль и NH4Cl). Они имеют вид табличек; от KHO и Н2O2 не темнеют. 3) NiC2O4+2H2O выделяется в очень мелких кристаллах.Серебро характеризуется главным образом в виде AgCl. Аморфный осадок хлористого серебра непригоден для микрохимического исследования; его растворяют в NH3 и кристаллизуют при медленном испарении NH3. Получаются очень мелкие кристаллы в виде куба или октаэдра, а также и комбинации их. Для растворения AgCl применяется также нагретая крепкая HCl. Из других соединений серебра, применяющихся при анализе, можно указать на хромовокислую соль (фиг. 17), углекислую, щавелевокислую и проч.
Фиг. 15.2) Очень характерна для Co двойная соль Co(CNS)2.Hg(CNS)2 — кристаллы синего цвета; в присутствии Zn и Cd выделяются смеси солей того же вида, слабо окрашенные в синий цвет (фиг. 16). 3) NH4CoPO4 получается так же, как для Mg; от KHO и Н2O2 окрашивается в темный цвет.Никель характеризуется тройной азотистокислой солью калия, никеля и свинца, двойной фосфорно-аммиачно-никелевой солью и щавелевокислой солью. 1) Растворы никелевых солей, подкисленные уксусной кислотой, с KNO2 и уксуснокислым свинцом дают желтые кристаллы K2NiPb(NO2)6, схожие с кристаллами азотисто-кобальто-калиевой соли. Pb может быть заменен Ba, Ca, Sr. 2) Кристаллы NH4NiPO4+2Н2О образуются в тех же условиях, как и для магния (однако, лучше брать углеаммиачную соль и NH4Cl). Они имеют вид табличек; от KHO и Н2O2 не темнеют. 3) NiC2O4+2H2O выделяется в очень мелких кристаллах.Серебро характеризуется главным образом в виде AgCl. Аморфный осадок хлористого серебра непригоден для микрохимического исследования; его растворяют в NH3 и кристаллизуют при медленном испарении NH3. Получаются очень мелкие кристаллы в виде куба или октаэдра, а также и комбинации их. Для растворения AgCl применяется также нагретая крепкая HCl. Из других соединений серебра, применяющихся при анализе, можно указать на хромовокислую соль (фиг. 17), углекислую, щавелевокислую и проч.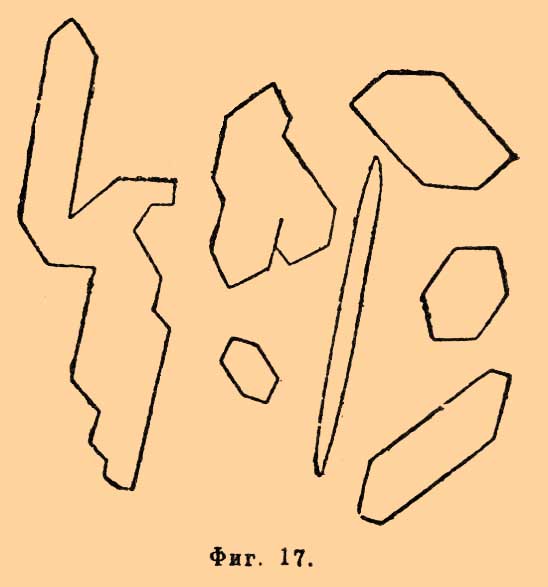 Фиг. 17.Медь определяется в виде тройной азотистокислой соли K2CuPb(NO2)6, двойной аммиачной железисто-синеродистой (NH3)4Cu2Fe(CN)6, двойной роданистой со ртутью Cu(CNS)2Hg(CNS)2 и в виде йодистой меди Cu2I2. 1) Для получения K2CuPb(NO2)6 берут концентрированный раствор медной соли, прибавляют туда уксусно-натриевой соли, каплю насыщенного раствора KNO2, подкисляют уксусной кислотой и кладут кристаллик уксуснокислого свинца. Тройная соль представляет кристаллы темно-оранжевого цвета в виде кубиков, как для Ni. Для получения хороших результатов необходим избыток KNO2. В присутствии CsCl и TlNO3 чувствительность реакции увеличивается. От NH3 окраска кристаллов исчезает и появляется вновь от уксусной кислоты. 2) Для получения (NH3)4Cu2Fe(CN)6 к раствору медной соли прибавляют NH3 и кристаллик желтой соли. При испарении NH3 выделяются древовидные кристаллы, слабо окрашенные в красный цвет. От уксусной кислоты они становятся ярко-красными. 3) Cu(CNS)2Hg(CNS)2 выделяется в характерных кристаллах (фиг. 18) при действии двойной соли роданистой ртути с роданистым аммонием.Фиг. 18.4) Cu2I2 выделяется в виде мелких зерен от действия KI. При слабых растворах осаждение ведется в присутствии восстановителей (сернистокислого натрия и Н2SO4).Ртуть. Для солей закиси характерна HgCl — белые зерна, чернеющие от NH3; в солях окиси ртуть определяется в виде йодной ртути HgI2, в виде каломели HgCl и в виде двойной роданистой Co(CNS)2Hg(CNS)2, описанной выше при кобальте. HgI2 получается в виде красных пластинок и пирамид, иногда же в виде иголочек (фиг. 19), при действии йодистого калия на соль окиси ртути. Кристаллы растворяются в избытке реактива.Фиг. 19. Фиг. 20. Фиг. 21.Кадмий определяется в виде углекислой соли CdCO3, щавелевокислой CdC2O4+3Н2O, двойной роданистой с роданистой ртутью и в виде железисто-синеродистой. 1) CdCO3 осаждается содой в виде мелких зерен. В присутствии Mg, Ni, Zn осаждение ведут в аммиачном растворе. 2) CdC2O4+3H2O выделяется в виде ромбоэдров и длинных табличек (фиг. 20). Присутствие кислот, солей алюминия, железа, хрома, цинка, никеля, магния вредит реакции. Обыкновенно поступают так: осаждают Cd из аммиачного раствора в виде CdCO3, промывают его и прибавляют к нему кристаллик щавелевой кислоты. 3) Cd(CNS)2. Hg(CNS)2 выделяется в виде прямоугольных призм и пирамид. 3) Железисто-синеродистый кадмий получается в виде желтого порошка или мелких кубиков.Свинец определяется в виде хлористого PbCl2, йодистого PbI2, сернокислого PbSO4, углекислого PbCO3 и тройной азотистокислой соли Cs2PbCu(NO2)6. 1) PbCl2 получают из сравнительно крепких растворов Pb — солей в виде тонких табличек (фиг. 21) при действии HCl. Присутствие других хлористых соединений вообще вредит, так как могут образоваться двойные соли. 2) PbI2 получается в виде шестиугольных таблиц лимонно-желтого цвета при действии KI на соли свинца; в избытке KI он растворяется. В присутствии солей висмута и сурьмы получается бурый порошок. 3) При осаждении серной кислотой или сернокислыми солями PbSO4 выделяется в аморфном виде. Он растворяется в нагретой HCl или HNO3 и при охлаждении отчасти кристаллизуется в виде мелких ромбоэдров и табличек подобно BaSO4. 4) PbCO3 образует характерные иголочки. 5) Образование Cs2PbCu(NO2)6 — см. выше при меди. Для характеристики свинца рекомендуют также щавелевокислую соль, хромовокислую и даже азотнокислую.Висмут характеризуется в виде двойной щавелевокислой соли с щавелевокислым калием, двойных соединений хлористого висмута с хлористыми рубидием или цезием и в виде двойной сернокислой соли 3K2SO4.Bi2(SO3)3. 1) Щавелевокислый калий в солях висмута осаждает бесцветные иголочки, которые при нагревании растворяются в избытке реактива и при охлаждении выделяются в виде пирамид (фиг. 22).Фиг. 22. Фиг. 23.2) С RbCl соединения висмута в присутствии HCl образуют характерные бесцветные таблички (фиг. 23). При очень слабых растворах и при избытке кислоты употребляется CsCl, дающий такие же кристаллы. KI увеличивает чувствительность этой реакции. О двойной сернокислой соли сказано выше при калии.Золото характеризуется осаждением хлористым оловом в виде двойного хлористого соединения с таллием и двойной роданисто-аммиачной соли. 1) При действии смеси SnCl2 и SnCl4 на раствор соли золота образуется красный мелкий осадок. Делается это таким образом, что каплю испытуемого раствора придвигают к капле реактива, причем в месте соприкосновения их получается красная полоска. 2) Азотнокислый таллий даже в слабом растворе AuCl3 дает место образованию AuTlCl4+5Н2O в виде палочек или щеточек желтого цвета (фиг. 24).
Фиг. 17.Медь определяется в виде тройной азотистокислой соли K2CuPb(NO2)6, двойной аммиачной железисто-синеродистой (NH3)4Cu2Fe(CN)6, двойной роданистой со ртутью Cu(CNS)2Hg(CNS)2 и в виде йодистой меди Cu2I2. 1) Для получения K2CuPb(NO2)6 берут концентрированный раствор медной соли, прибавляют туда уксусно-натриевой соли, каплю насыщенного раствора KNO2, подкисляют уксусной кислотой и кладут кристаллик уксуснокислого свинца. Тройная соль представляет кристаллы темно-оранжевого цвета в виде кубиков, как для Ni. Для получения хороших результатов необходим избыток KNO2. В присутствии CsCl и TlNO3 чувствительность реакции увеличивается. От NH3 окраска кристаллов исчезает и появляется вновь от уксусной кислоты. 2) Для получения (NH3)4Cu2Fe(CN)6 к раствору медной соли прибавляют NH3 и кристаллик желтой соли. При испарении NH3 выделяются древовидные кристаллы, слабо окрашенные в красный цвет. От уксусной кислоты они становятся ярко-красными. 3) Cu(CNS)2Hg(CNS)2 выделяется в характерных кристаллах (фиг. 18) при действии двойной соли роданистой ртути с роданистым аммонием.Фиг. 18.4) Cu2I2 выделяется в виде мелких зерен от действия KI. При слабых растворах осаждение ведется в присутствии восстановителей (сернистокислого натрия и Н2SO4).Ртуть. Для солей закиси характерна HgCl — белые зерна, чернеющие от NH3; в солях окиси ртуть определяется в виде йодной ртути HgI2, в виде каломели HgCl и в виде двойной роданистой Co(CNS)2Hg(CNS)2, описанной выше при кобальте. HgI2 получается в виде красных пластинок и пирамид, иногда же в виде иголочек (фиг. 19), при действии йодистого калия на соль окиси ртути. Кристаллы растворяются в избытке реактива.Фиг. 19. Фиг. 20. Фиг. 21.Кадмий определяется в виде углекислой соли CdCO3, щавелевокислой CdC2O4+3Н2O, двойной роданистой с роданистой ртутью и в виде железисто-синеродистой. 1) CdCO3 осаждается содой в виде мелких зерен. В присутствии Mg, Ni, Zn осаждение ведут в аммиачном растворе. 2) CdC2O4+3H2O выделяется в виде ромбоэдров и длинных табличек (фиг. 20). Присутствие кислот, солей алюминия, железа, хрома, цинка, никеля, магния вредит реакции. Обыкновенно поступают так: осаждают Cd из аммиачного раствора в виде CdCO3, промывают его и прибавляют к нему кристаллик щавелевой кислоты. 3) Cd(CNS)2. Hg(CNS)2 выделяется в виде прямоугольных призм и пирамид. 3) Железисто-синеродистый кадмий получается в виде желтого порошка или мелких кубиков.Свинец определяется в виде хлористого PbCl2, йодистого PbI2, сернокислого PbSO4, углекислого PbCO3 и тройной азотистокислой соли Cs2PbCu(NO2)6. 1) PbCl2 получают из сравнительно крепких растворов Pb — солей в виде тонких табличек (фиг. 21) при действии HCl. Присутствие других хлористых соединений вообще вредит, так как могут образоваться двойные соли. 2) PbI2 получается в виде шестиугольных таблиц лимонно-желтого цвета при действии KI на соли свинца; в избытке KI он растворяется. В присутствии солей висмута и сурьмы получается бурый порошок. 3) При осаждении серной кислотой или сернокислыми солями PbSO4 выделяется в аморфном виде. Он растворяется в нагретой HCl или HNO3 и при охлаждении отчасти кристаллизуется в виде мелких ромбоэдров и табличек подобно BaSO4. 4) PbCO3 образует характерные иголочки. 5) Образование Cs2PbCu(NO2)6 — см. выше при меди. Для характеристики свинца рекомендуют также щавелевокислую соль, хромовокислую и даже азотнокислую.Висмут характеризуется в виде двойной щавелевокислой соли с щавелевокислым калием, двойных соединений хлористого висмута с хлористыми рубидием или цезием и в виде двойной сернокислой соли 3K2SO4.Bi2(SO3)3. 1) Щавелевокислый калий в солях висмута осаждает бесцветные иголочки, которые при нагревании растворяются в избытке реактива и при охлаждении выделяются в виде пирамид (фиг. 22).Фиг. 22. Фиг. 23.2) С RbCl соединения висмута в присутствии HCl образуют характерные бесцветные таблички (фиг. 23). При очень слабых растворах и при избытке кислоты употребляется CsCl, дающий такие же кристаллы. KI увеличивает чувствительность этой реакции. О двойной сернокислой соли сказано выше при калии.Золото характеризуется осаждением хлористым оловом в виде двойного хлористого соединения с таллием и двойной роданисто-аммиачной соли. 1) При действии смеси SnCl2 и SnCl4 на раствор соли золота образуется красный мелкий осадок. Делается это таким образом, что каплю испытуемого раствора придвигают к капле реактива, причем в месте соприкосновения их получается красная полоска. 2) Азотнокислый таллий даже в слабом растворе AuCl3 дает место образованию AuTlCl4+5Н2O в виде палочек или щеточек желтого цвета (фиг. 24). Фиг. 24.Нагревание ускоряет образование их; но при этом может выделяться золото в металлическом виде. Двойная роданисто-аммиачная соль золота подобна ртутной.Платина характеризуется, главным образом, образованием хлороплатинатов калия, рубидия, цезия и таллия. Все они по внешнему виду более или менее сходны.Олово в солях закиси (SnCl2) характеризуется восстановительными реакциями с AuCl3 и HgCl2, а в солях окиси (SnCl4) образованием CsSnCl6 (см. выше при цезии).Сурьма характеризуется образованием двойной хлористо-водородной соли с CsCl, двойной винно-бариевой соли и пиросурьмяно-натриевой. 1) CsCl в растворах солей сурьмы в соляной кислоте дает прозрачные шестиугольные таблички Cs2SbCl4+2,5H2O, подобно тому как при висмуте (фиг. 25).Фиг. 25. Фиг. 26.Если сурьма находится в растворе в смеси с висмутом, то сначала образуется BiCs2Cl+2,5H2O. KI и здесь увеличивает чувствительность реакции. 2) При прибавлении к нагретому раствору сурьмяной соли виннокислого бария образуются таблички BaC4H4O6(SbO)2.C4H4O6+2H2O. 3) Для получения пиросурьмяно-натриевой соли исследуемое вещество окисляют, сплавляя с калийной селитрой, при нагревании извлекают водой и раствор осаждают с помощью NaCl. Эта реакция очень характерна для сурьмы.Мышьяк определяется в виде соединений мышьяковой кислоты. Низшие степени окисления мышьяка переводятся в высшие окислением смесью соляной кислоты с бертолетовой солью. Для него характерна двойная аммиачно-кальциевая соль мышьяковой кислоты и мышьяково-молибденово-аммиачная соль. 1) Раствор мышьяковой кислоты насыщают аммиаком и прибавляют уксуснокислого кальция; получающиеся при этом кристаллы NH4CaAsO4+6H2О сходны с фосфорно-аммиачно-магнезиальной солью. Присутствие аммиачных солей вредит чувствительности. Вместо кальция можно также взять соль магния или цинка; форма кристаллов одна и та же. 2) С молибденовокислым аммиаком, в особенности при нагревании, образуются кристаллы (NH4)3AsO4+10MoO3+3H2O. Кристаллы схожи с фосфорно-молибденовокислым калием. Если присутствует фосфорная кислота, то сначала выделяется она, а потом уже мышьяковая.Фосфор в форме P2O5 характеризуется образованием двойной фосфорно-аммиачно-магнезиальной соли (см. выше) и фосфорно-молибденового аммония, сходного с соответственной калийной солью.Азот. В NH3 характеризуется образованием хлороплатината (NH4PtCl6, схожего с K2PtCl6, фосфорно-аммиачно-магнезиальной соли и хлористого меркураммония. Для выделения аммиака исследуемое вещество выпаривают с соляной кислотой, кладут в платиновую ложечку и смачивают крепким раствором NaHO; сюда же кладут немного асбеста, который впитывает в себя всю жидкость; затем ложечку закрывают стеклянной пластинкой, на которой находится капля слабой соляной кислоты (так, чтобы кислота была внутри ложечки), и нагревают на маленьком пламени, пока ок. кислоты не образуется налет; поверх пластинки для охлаждения кладут каплю воды или спирта. Азот в HNO3 и ее солях характеризуется или в виде аммиака, восстановляя HNO3 цинком с KHO, или переводя HNO3 в HNO2 и выделяя последней йод из KI в присутствии крахмала. Для перевода азотнокислых солей в азотистокислые их нагревают в нейтральном растворе с порошком магния. После восстановления их подкисляют слегка серной кислотой и прибавляют сюда KI и крахмала. Цианистые соединения определяются в виде берлинской лазури.Сера определяется в виде солей серной кислоты. Для окисления различных сернистых соединений пользуются сплавлением их с селитрой, действием дымящей HNO3 и бромной воды. Н2SO4 характеризуется получением гипса, цезиевых квасцов и сернокислого свинца.Галоиды. Хлор, бром, йод и фтор. Для хлора характерны соединения с таллием TlCl, с серебром AgCl, хлороплатинаты таллия и калия Tl2PtCl6 и K2PtCl6. Обыкновенно выделяют HCl, нагревая исследуемое вещество с Н2SO4 и улавливая ее подобно тому, как при аммиаке, причем для поглощения ее пользуются KHO. Бром характеризуется такими же бромистыми соединениями, очень похожими на вышеописанные. Йод характеризуется, главным образом, синим соединением с крахмалом; кроме того, для него характерны TlI, AgI, K2PtI6, HgI2, отличающиеся от соединений хлора и брома своей окраской. Для фтора характерны Na2SiF6 и BaSiF6. К исследуемому веществу прибавляют HCl и кремнекислоты и пробуют хлористым натрием или барием, часто приходится отгонять кремнефтористо-водородную кислоту, нагревая вещество с крепкой Н2SO4 в присутствии кремнекислоты в платиновой ложечке; для поглощения служит капля Н2SO4.Бор определяется, главным образом, в виде KBF4. Вещество растворяют в HF или в HCl с NH4F и прибавляют немного KCl. При сгущении выделяются ромбические таблички или призмы с пирамидами на концах (фиг. 26). Кремний мешает реакции и должен быть удален выпариванием с HF на водяной бане или осаждением уксуснокислым барием.Кремний определяется в виде кремнефтористого натрия Na2SiF6 и в виде кремнемолибденового рубидия. 1) Проба растворяется в HF или в HCl с NH4F и к ней прибавляется NaCl. При отсутствии Н2SO4 получают кремнефтористый барий, дающий более крупные кристаллы. 2) Вещество сплавляют с содой, сплав растворяют в воде и прибавляют молибденового аммиака и азотной кислоты в избытке, нагревают, чтобы облегчить осаждение кислот фосфорной, мышьяковой и проч., и затем, охладив, в прозрачную жидкость прибавляют RbCl. Образуются зернышки кремнемолибдата рубидия. Реакция очень чувствительна, но подобные же соединения дают ванадий, молибден, висмут и проч.Углерод в форме СО2. В растворимых солях СО2 характеризуется образованием СаСО3, PbCO3, SrCO3; из нерастворимых СО2 выделяется в газообразном виде соляной кислотой. Если вещества немного, его кладут в каплю воды на стекло, закрывают стеклышком и, придвинув к одному углу стеклышка каплю слабой HCl, с противоположного угла высасывают бумагой воду, чтобы ввести HCl под стекло. В микроскоп наблюдают появление пузырьков СО2. Образцы, могущие содержать вещества органические, осторожно сжигаются с селитрой и затем испытываются на СО2. Водород и кислород опр. в виде Н2О.Ход микрохимического исследования. I. Имеется жидкость: а) пробуют реакцию ее (кислую или щелочную). Для этого берут каплю ее платиновой проволочкой и проводят ей черточку по реагентной бумаге. Если жидкости немного, в нее кладут крупинку индикатора (лакмуса, Kongoroth и проч.); b) испытывают летучесть. Каплю жидкости кладут на стекло; на него помещают маленький треугольник из проволочки и стекла так, чтобы капля пришлась в середине. На треугольник кладут покровное стеклышко с каплей соответственного реактива и слегка подогревают стекло. Н2S открывают уксуснокислым кадмием; HCl, HBr, HI — азотнокислым таллием; HNO3, HNO2, Cl — по выделению йода из KI; HCN — по образованию берлинской лазури; SO2 — после окисления в виде Н2SO4; NH3 — в виде хлороплатината и проч.; с) жидкость выпаривают, чтобы узнать, заключает ли она в растворе твердые вещества. При этом не надо забывать, что твердый остаток может получиться из стекла, в котором сохранялась жидкость или взятые реагенты; поэтому делают соответственные испытания их и проч.II. Имеется твердое вещество. Пробуют: а) растворить его, b) сублимировать. а) Пробуют сначала растворить в воде; если не растворяется, прибегают к HCl, HNO3 или их смеси, к H2SO4 и проч., как в обыкновенном анализе; b) для сублимации вещество кладут на проволоку с расплющенным концом и осторожно нагревают на горелке; при этом стараются, чтобы пары вещества садились на стеклянную пластинку, которую держат над проволочкой. Если вещество состоит из окисей, то улетучивается As2О3, Sb2O3, окись ртути дает налет металлической ртути и проч. Иногда вещество обрабатывают HCl и сублимируют. Легко улетучиваются CdCl2, BiCl3, ZnCl2, CuCl2, PbCl2 и проч. При навыке по характеру налета можно сделать некоторые выводы, а отчасти этим путем можно произвести разделение. Получив такими предварительными испытаниями понятие об исследуемом веществе, пробуют произвести разделение, получая галоидные соединения, сернокислые соли, углекислые, щавелевокислые и проч. и изучая их свойства. Общие указания здесь дать трудно. Приходится ориентироваться в зависимости от обстоятельств. Прекрасным руководством при микрохимических исследованиях может служить Behrens, "Anleitung zur Mikrochemischen Analyse".С. Вуколов. Δ.
Фиг. 24.Нагревание ускоряет образование их; но при этом может выделяться золото в металлическом виде. Двойная роданисто-аммиачная соль золота подобна ртутной.Платина характеризуется, главным образом, образованием хлороплатинатов калия, рубидия, цезия и таллия. Все они по внешнему виду более или менее сходны.Олово в солях закиси (SnCl2) характеризуется восстановительными реакциями с AuCl3 и HgCl2, а в солях окиси (SnCl4) образованием CsSnCl6 (см. выше при цезии).Сурьма характеризуется образованием двойной хлористо-водородной соли с CsCl, двойной винно-бариевой соли и пиросурьмяно-натриевой. 1) CsCl в растворах солей сурьмы в соляной кислоте дает прозрачные шестиугольные таблички Cs2SbCl4+2,5H2O, подобно тому как при висмуте (фиг. 25).Фиг. 25. Фиг. 26.Если сурьма находится в растворе в смеси с висмутом, то сначала образуется BiCs2Cl+2,5H2O. KI и здесь увеличивает чувствительность реакции. 2) При прибавлении к нагретому раствору сурьмяной соли виннокислого бария образуются таблички BaC4H4O6(SbO)2.C4H4O6+2H2O. 3) Для получения пиросурьмяно-натриевой соли исследуемое вещество окисляют, сплавляя с калийной селитрой, при нагревании извлекают водой и раствор осаждают с помощью NaCl. Эта реакция очень характерна для сурьмы.Мышьяк определяется в виде соединений мышьяковой кислоты. Низшие степени окисления мышьяка переводятся в высшие окислением смесью соляной кислоты с бертолетовой солью. Для него характерна двойная аммиачно-кальциевая соль мышьяковой кислоты и мышьяково-молибденово-аммиачная соль. 1) Раствор мышьяковой кислоты насыщают аммиаком и прибавляют уксуснокислого кальция; получающиеся при этом кристаллы NH4CaAsO4+6H2О сходны с фосфорно-аммиачно-магнезиальной солью. Присутствие аммиачных солей вредит чувствительности. Вместо кальция можно также взять соль магния или цинка; форма кристаллов одна и та же. 2) С молибденовокислым аммиаком, в особенности при нагревании, образуются кристаллы (NH4)3AsO4+10MoO3+3H2O. Кристаллы схожи с фосфорно-молибденовокислым калием. Если присутствует фосфорная кислота, то сначала выделяется она, а потом уже мышьяковая.Фосфор в форме P2O5 характеризуется образованием двойной фосфорно-аммиачно-магнезиальной соли (см. выше) и фосфорно-молибденового аммония, сходного с соответственной калийной солью.Азот. В NH3 характеризуется образованием хлороплатината (NH4PtCl6, схожего с K2PtCl6, фосфорно-аммиачно-магнезиальной соли и хлористого меркураммония. Для выделения аммиака исследуемое вещество выпаривают с соляной кислотой, кладут в платиновую ложечку и смачивают крепким раствором NaHO; сюда же кладут немного асбеста, который впитывает в себя всю жидкость; затем ложечку закрывают стеклянной пластинкой, на которой находится капля слабой соляной кислоты (так, чтобы кислота была внутри ложечки), и нагревают на маленьком пламени, пока ок. кислоты не образуется налет; поверх пластинки для охлаждения кладут каплю воды или спирта. Азот в HNO3 и ее солях характеризуется или в виде аммиака, восстановляя HNO3 цинком с KHO, или переводя HNO3 в HNO2 и выделяя последней йод из KI в присутствии крахмала. Для перевода азотнокислых солей в азотистокислые их нагревают в нейтральном растворе с порошком магния. После восстановления их подкисляют слегка серной кислотой и прибавляют сюда KI и крахмала. Цианистые соединения определяются в виде берлинской лазури.Сера определяется в виде солей серной кислоты. Для окисления различных сернистых соединений пользуются сплавлением их с селитрой, действием дымящей HNO3 и бромной воды. Н2SO4 характеризуется получением гипса, цезиевых квасцов и сернокислого свинца.Галоиды. Хлор, бром, йод и фтор. Для хлора характерны соединения с таллием TlCl, с серебром AgCl, хлороплатинаты таллия и калия Tl2PtCl6 и K2PtCl6. Обыкновенно выделяют HCl, нагревая исследуемое вещество с Н2SO4 и улавливая ее подобно тому, как при аммиаке, причем для поглощения ее пользуются KHO. Бром характеризуется такими же бромистыми соединениями, очень похожими на вышеописанные. Йод характеризуется, главным образом, синим соединением с крахмалом; кроме того, для него характерны TlI, AgI, K2PtI6, HgI2, отличающиеся от соединений хлора и брома своей окраской. Для фтора характерны Na2SiF6 и BaSiF6. К исследуемому веществу прибавляют HCl и кремнекислоты и пробуют хлористым натрием или барием, часто приходится отгонять кремнефтористо-водородную кислоту, нагревая вещество с крепкой Н2SO4 в присутствии кремнекислоты в платиновой ложечке; для поглощения служит капля Н2SO4.Бор определяется, главным образом, в виде KBF4. Вещество растворяют в HF или в HCl с NH4F и прибавляют немного KCl. При сгущении выделяются ромбические таблички или призмы с пирамидами на концах (фиг. 26). Кремний мешает реакции и должен быть удален выпариванием с HF на водяной бане или осаждением уксуснокислым барием.Кремний определяется в виде кремнефтористого натрия Na2SiF6 и в виде кремнемолибденового рубидия. 1) Проба растворяется в HF или в HCl с NH4F и к ней прибавляется NaCl. При отсутствии Н2SO4 получают кремнефтористый барий, дающий более крупные кристаллы. 2) Вещество сплавляют с содой, сплав растворяют в воде и прибавляют молибденового аммиака и азотной кислоты в избытке, нагревают, чтобы облегчить осаждение кислот фосфорной, мышьяковой и проч., и затем, охладив, в прозрачную жидкость прибавляют RbCl. Образуются зернышки кремнемолибдата рубидия. Реакция очень чувствительна, но подобные же соединения дают ванадий, молибден, висмут и проч.Углерод в форме СО2. В растворимых солях СО2 характеризуется образованием СаСО3, PbCO3, SrCO3; из нерастворимых СО2 выделяется в газообразном виде соляной кислотой. Если вещества немного, его кладут в каплю воды на стекло, закрывают стеклышком и, придвинув к одному углу стеклышка каплю слабой HCl, с противоположного угла высасывают бумагой воду, чтобы ввести HCl под стекло. В микроскоп наблюдают появление пузырьков СО2. Образцы, могущие содержать вещества органические, осторожно сжигаются с селитрой и затем испытываются на СО2. Водород и кислород опр. в виде Н2О.Ход микрохимического исследования. I. Имеется жидкость: а) пробуют реакцию ее (кислую или щелочную). Для этого берут каплю ее платиновой проволочкой и проводят ей черточку по реагентной бумаге. Если жидкости немного, в нее кладут крупинку индикатора (лакмуса, Kongoroth и проч.); b) испытывают летучесть. Каплю жидкости кладут на стекло; на него помещают маленький треугольник из проволочки и стекла так, чтобы капля пришлась в середине. На треугольник кладут покровное стеклышко с каплей соответственного реактива и слегка подогревают стекло. Н2S открывают уксуснокислым кадмием; HCl, HBr, HI — азотнокислым таллием; HNO3, HNO2, Cl — по выделению йода из KI; HCN — по образованию берлинской лазури; SO2 — после окисления в виде Н2SO4; NH3 — в виде хлороплатината и проч.; с) жидкость выпаривают, чтобы узнать, заключает ли она в растворе твердые вещества. При этом не надо забывать, что твердый остаток может получиться из стекла, в котором сохранялась жидкость или взятые реагенты; поэтому делают соответственные испытания их и проч.II. Имеется твердое вещество. Пробуют: а) растворить его, b) сублимировать. а) Пробуют сначала растворить в воде; если не растворяется, прибегают к HCl, HNO3 или их смеси, к H2SO4 и проч., как в обыкновенном анализе; b) для сублимации вещество кладут на проволоку с расплющенным концом и осторожно нагревают на горелке; при этом стараются, чтобы пары вещества садились на стеклянную пластинку, которую держат над проволочкой. Если вещество состоит из окисей, то улетучивается As2О3, Sb2O3, окись ртути дает налет металлической ртути и проч. Иногда вещество обрабатывают HCl и сублимируют. Легко улетучиваются CdCl2, BiCl3, ZnCl2, CuCl2, PbCl2 и проч. При навыке по характеру налета можно сделать некоторые выводы, а отчасти этим путем можно произвести разделение. Получив такими предварительными испытаниями понятие об исследуемом веществе, пробуют произвести разделение, получая галоидные соединения, сернокислые соли, углекислые, щавелевокислые и проч. и изучая их свойства. Общие указания здесь дать трудно. Приходится ориентироваться в зависимости от обстоятельств. Прекрасным руководством при микрохимических исследованиях может служить Behrens, "Anleitung zur Mikrochemischen Analyse".С. Вуколов. Δ.
Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона. — С.-Пб.: Брокгауз-Ефрон. 1890—1907.