- Оксид азота (III)
-
Оксид азота(III) 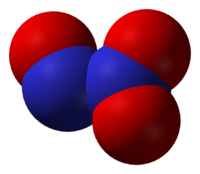
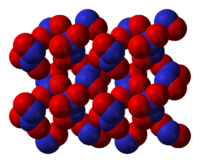
Общие Систематическое наименование Оксид азота(III) Химическая формула N2O3 Отн. молек. масса 30.0061 а. е. м. Молярная масса 30.0061 г/моль Физические свойства Плотность вещества 1.4 × 103 кг м−3, жидкость г/см³ Состояние (ст. усл.) бесцветный газ Термические свойства Температура плавления −100.1 °C Температура кипения −40 °C Энтальпия (ст. усл.) 81 кДж/моль Химические свойства Растворимость в воде 0,01 г/100 мл Классификация номер CAS [10544-73-7]
Окси́д азо́та(III) (азотистый ангидрид, сесквиоксид азота) N2O3 — бесцветный газ (при н. у.), в твёрдом виде слабо-синего цвета. Устойчив только при температурах ниже −101 °C. Без примесей NO2 и NO он существует только в твёрдом виде.Содержание
Получение
Рекомендуется капать 50%-ю азотную кислоту на твёрдый оксид мышьяка(III):
- 2HNO3 (50 %) + As2O3 → NO2↑ + NO↑ + HAsO3.
N2O3 образуется при охлаждении получающейся смеси газов.
При пропускании электрического разряда через жидкий воздух N2O3 можно получить в виде порошка голубого цвета:
- N2 + O2 → 2NO;
- 2NO + O2 → 2NO2;
- NO + 2NO2 → N2O3.
Также N2O3 можно получить действием 50%-ой азотной кислоты на крахмал.
Химические свойства
Кислотный оксид. N2O3 подвержен термической диссоциации:
- N2O3 ↔ NO2 + NO.
При 25 °C содержание N2O3 в смеси газов составляет около 10,5 %. Жидкий оксид азота (III) синего цвета, он также частично диссоциирован.
Являясь азотистым ангидридом, при взаимодействии с водой N2O3 даёт азотистую кислоту:
- N2O3 + H2O ↔ 2HNO2.
При взаимодействии с растворами щелочей образуются соответствующие нитриты:
- N2O3 + 2KOH → 2KNO2 + H2O.
Применение
Применяется в лаборатории для получения азотистой кислоты и её солей.
Физиологическое действие
Высоко токсичен. По действию на организм сравним с дымящей азотной кислотой. Вызывает тяжёлые ожоги кожи.
Wikimedia Foundation. 2010.
