- европий
- ЕВРО́ПИЙ -ия; м. [лат. Europium] Химический элемент (Eu), радиоактивный металл серебристо-белого цвета, относящийся к лантаноидам (получается искусственным путём; используется в ядерной и радиотехнической промышленности).* * *евро́пий(лат. Europium), химический элемент III группы периодической системы, относится к лантаноидам. Металл, плотность 5,245 г/см3, tпл 826°C. Название от «Европа» (часть света). Поглотитель нейтронов в ядерных реакторах, активатор люминофоров в цветных телевизорах.
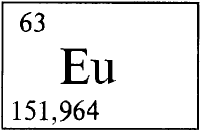 * * *ЕВРОПИЙЕВРО́ПИЙ (лат. Europium), Eu (читается «европий»), химический элемент с атомным номером 63, атомная масса 151,96. Состоит из двух стабильных изотопов 151Eu (47,82%) и 153Eu (52,18%). Конфигурация внешних электронных слоев 4s2p6d10f75s2p66s2. Степень окисления в соединениях +3 (валентность III), реже +2 (валентность II).
* * *ЕВРОПИЙЕВРО́ПИЙ (лат. Europium), Eu (читается «европий»), химический элемент с атомным номером 63, атомная масса 151,96. Состоит из двух стабильных изотопов 151Eu (47,82%) и 153Eu (52,18%). Конфигурация внешних электронных слоев 4s2p6d10f75s2p66s2. Степень окисления в соединениях +3 (валентность III), реже +2 (валентность II).
Относится к редкоземельным элементам (цериевая подгруппа лантаноидов). Расположен в группе III B, в 6 периоде периодической системы. Радиус нейтрального атома 0,202 нм, радиус иона Eu2+ — 0,131 нм, иона Eu3+— 0,109 нм. Энергии ионизации 5,664, 11,25, 24,70, 42,65 эВ. Электроотрицательность по Полингу (см. ПОЛИНГ Лайнус) 1.
История открытия
Европий открыт Э. Демарсе в 1886. Название элемент получил в 1901 по названию континента. Металлический европий был впервые получен в 1937 году.
Нахождение в природе
Содержание европия в земной коре 1,310 -4%, в морской воде 1,110 -6мг/л. Входит в состав минералов монацита (см. МОНАЦИТ), лопарита (см. ЛОПАРИТ), бастнезита (см. БАСТНЕЗИТ) и других.
Получение
Металлический европий получают восстановлением Eu2О3 в вакууме лантаном или углеродом, а также электролизом расплава EuСl3.
Физические и химические свойства
Европий — серебристо-серый металл. Решетка кубическая типа a-Fe, а = 0,4582 нм. Температура плавления 826 °C, температура кипения 1559 °C, плотность 5,245 кг/дм3.
На воздухе европий покрывается пленкой оксидов и гидратированных карбонатов. При небольшом нагревании окисляется быстро. При слабом нагревании реагирует с галогенами, азотом и водородом. С водой и минеральными кислотами реагирует при комнатной температуре.
Оксид Eu2О3 обладает основными свойствами, ему отвечает сильное основание Eu(ОН)3. При взаимодействии Eu и Eu2О3, а также при взаимодействии оксигалогенидов трехвалентного европия с гидридом лития LiH образуется оксид европия (II) EuО. Этому оксиду отвечает основание Eu(ОН)2.
Применение
Применяют как поглотитель нейтронов в ядерной технике, активатор люминофоров красного свечения, используемых в цветном телевидении. 155Eu — в медицинской диагностике.
Энциклопедический словарь. 2009.
