- Бром
-
(лат. Bromum)
Br, химический элемент VII группы периодической системы Менделеева, относится к галогенам (См. Галогены); атомный номер 35, атомная масса 79,904; красно-бурая жидкость с сильным неприятным запахом. Б. открыт в 1826 французским химиком А. Ж. Баларом при изучении рассолов средиземноморских соляных промыслов; назван от греческого bromos — зловоние. Природный Б. состоит из 2 стабильных изотопов 79Br (50,54%) и 81Вг (49,46%). Из искусственно полученных радиоактивных изотопов Б. наиболее интересен 80Br, на примере которого И. В. Курчатовым открыто явление изомерии атомных ядер (См. Изомерия атомных ядер).Нахождение в природе. Содержание Б. в земной коре (1,6·10-4% по массе) оценивается в 1015—1016 т. В главной своей массе Б. находится в рассеянном состоянии в магматических породах, а также в широко распространённых галогенидах. Б. — постоянный спутник хлора. Бромистые соли (NaBr, KBr, MgBr2) встречаются в отложениях хлористых солей (в поваренной соли до 0,03% Br, в калийных солях — сильвине и карналлите — до 0,3% Br), а также в морской воде (0,065% Br), рапе соляных озёр (до 0,2% Br) и подземных рассолах, обычно связанных с соляными и нефтяными месторождениями (до 0,1% Br). Благодаря хорошей растворимости в воде бромистые соли накопляются в остаточных рассолах морских и озёрных водоёмов. Б. мигрирует в виде легко растворимых соединений, очень редко образуя твёрдые минеральные формы, представленные бромиритом AgBr, эмболитом Ag (Cl, Br) и иодэмболитом Ag (Cl, Br, I). Образование минералов происходит в зонах окисления сульфидных серебросодержащих месторождений, формирующихся в засушливых пустынных областях. См. также Бромиды природные.Физические и химические свойства. При —7,2°С жидкий Б. застывает, превращаясь в красно-коричневые игольчатые кристаллы со слабым металлическим блеском. Пары Б. жёлто-бурого цвета, tkип 58,78°С. Плотность жидкого Б. (при 20°С) 3,1 г/см3. В воде Б. растворим ограниченно, но лучше других галогенов (3,58 г Б. в 100 г H2O при 20°С). Ниже 5,84°С из воды осаждаются гранатово-красные кристаллы Br2·8H2O. Особенно хорошо растворим Б. во многих органических растворителях, чем пользуются для извлечения его из водных растворов. Б. в твёрдом, жидком и газообразном состоянии состоит из 2-атомных молекул. Заметная диссоциация на атомы начинается при температуре около 800 °С; диссоциация наблюдается и при действии света.Конфигурация внешних электронов атома Б. 4s24p5 Валентность Б. в соединениях переменна, степень окисления равна — 1 (в бромидах, например KBr), + 1 (в гипобромитах, NaBrO), + 3 (в бромитах, NaBrO4), + 5 (в броматах, KBrO3) и + 7 (в перброматах, NaBrO4). Химически Б. весьма активен, занимая по реакционной способности место между хлором и йодом. Взаимодействие Б. с серой, селеном, теллуром, фосфором, мышьяком и сурьмой сопровождается сильным разогреванием, иногда даже появлением пламени. Так же энергично Б. реагирует с некоторыми металлами, например калием и алюминием. Однако многие металлы реагируют с безводным Б. с трудом из-за образования на их поверхности защитной плёнки бромида, нерастворимого в Б. Из металлов наиболее устойчивы к действию Б., даже при повышенных температурах и в присутствии влаги, серебро, свинец, платина и тантал (золото, в отличие от платины, энергично реагирует с Б.). С кислородом, азотом и углеродом Б. непосредственно не соединяется даже при повышенных температурах. Соединения Б. с этими элементами получают косвенным путём. Таковы крайне непрочные окислы Br2O, BrO2 и Br3O8 (последний получают, например, действием озона на Б. при 80°С). С галогенами Б. взаимодействует непосредственно, образуя BrF3, BrF5, BrCl, IBr и др. (см. Межгалогенные соединения).Б. — сильный окислитель. Так, он окисляет сульфиты и тиосульфаты в водных растворах до сульфатов, нитриты до нитратов, аммиак до свободного азота (3Вr2 + 8MH3 = N2 + 6NH4Br). Б. вытесняет йод из его соединений, но сам вытесняется хлором и фтором. Свободный Б. выделяется из водных растворов бромидов также под действием сильных окислителей (KMnO4, K2Cr2O7) в кислой среде. При растворении в воде Б. частично реагирует с ней
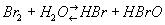 с образованием бромистоводородной кислоты HBr и неустойчивой бромноватистой кислоты (См. Бромноватистая кислота) HBrO. Раствор Б. в воде называется бромной водой (См. Бромная вода). При растворении Б. в растворах щелочей на холоду происходит образование бромида и гипобромита (2NaOH + Br2 = NaBr + NaBrO + H2O), а при повышенных температурах (около 100°С) — бромида и бромата (6NaOH + 3Br2 = 5NaBr + NaBrO3 + ЗН2О). Из реакций Б. с органическими соединениями наиболее характерны присоединение по двойной связи С=С, а также замещение водорода (обычно при действии катализаторов или света).Получение и применение. Исходным сырьём для получения Б. служат морская вода, озёрные и подземные рассолы и щелока калийного производства, содержащие Б. в виде бромид-иона Br- (от 65 г/м3 в морской воде до 3—4 кг/м3 и выше в щелоках калийного производства). Б. выделяют при помощи хлора (2Вг- + Cl2 = Br2 + 2С1-) и отгоняют из раствора водяным паром или воздухом. Отгонку паром ведут в колоннах, изготовленных из гранита, керамики или иного стойкого к Б. материала. Сверху в колонну подают подогретый рассол, а снизу — хлор и водяной пар. Пары Б., выходящие из колонны, конденсируют в керамиковых холодильниках. Далее Б. отделяют от воды и очищают от примеси хлора дистилляцией. Отгонка воздухом позволяет использовать для получения Б. рассолы с его низким содержанием, выделять Б. из которых паровым способом в результате большого расхода пара невыгодно. Из получаемой бромовоздушной смеси Б. улавливают химическими поглотителями. Для этого применяют растворы бромистого железа (2 FeBr2 + Br2 = 2FeBr3), которое, в свою очередь, получают восстановлением FeBr3 железными стружками, а также растворы гидроокисей или карбонатов натрия или газообразный сернистый ангидрид, реагирующий с Б. в присутствии паров воды с образованием бромистоводородной и серной кислот (Br2 + 3O2 + 2H2O = 2HBr + H2SO4). Из полученных полупродуктов Б. выделяют действием хлора (из FeBr3 и HBr) или кислоты (5NaBr + NaBrO3 + 3Н2SO4 = 3Вr2 + 3Na2SO4 + 3Н2О). В случае необходимости полупродукты перерабатывают на бромистые соединения, не выделяя элементарного Б.Вдыхание паров Б. при содержании их в воздухе 1 мг/м3 и более вызывает кашель, насморк, носовое кровотечение, головокружение, головную боль; при более высоких концентрациях — удушье, бронхит, иногда смерть. Предельно допустимые концентрации паров Б. в воздухе 2 мг/м3. Жидкий Б. действует на кожу, вызывая плохо заживающие ожоги. Работы с Б. следует проводить в вытяжных шкафах. При отравлении парами Б. рекомендуется вдыхать аммиак, используя для этой цели сильно разбавленный раствор его в воде или в этиловом спирте. Боль в горле, вызванную вдыханием паров Б., устраняют приёмом внутрь горячего молока. Б., попавший на кожу, смывают большим количеством воды или сдувают сильной струей воздуха. Обожжённые места смазывают ланолином.Б. применяют довольно широко. Он — исходный продукт для получения ряда бромистых солей и органических производных. Большие количества Б. расходуют для получения бромистого этила и ди-бромэтана — составных частей этиловой жидкости, добавляемой к бензинам для повышения их детонационной стойкости (см. Антидетонаторы). Соединения Б. применяют в фотографии, при производстве ряда красителей, бромистый метил и некоторые другие соединения Б. — как инсектициды. Некоторые органические соединения Б. служат эффективными огнетушащими средствами. Б. и бромную воду используют при химических анализах для определения многих веществ. В медицине используют бромиды натрия, калия, аммония, а также органические соединения Б., которые применяют при неврозах, истерии, повышенной раздражительности, бессоннице, гипертонической болезни, эпилепсии и хорее.Лит.: Ксензенко В. И., Стасиневич Д. С., Технология брома и йода, М., 1960; Позин М. Е., Технология минеральных солей, 2 изд., Л., 1961; Bromine and its compounds, ed. Z. Е. Jolles, L., 1966.В. К. Бельский, Д. С. Стасиневич.Бром в организме. Б. — постоянная составная часть тканей животных и растений. Наземные растения содержат в среднем 7·10-4% Б. на сырое вещество, животные Бром1·10-4%/ Б. найден в различных секретах (слезах, слюне, поте, молоке, желчи). В крови здорового человека содержание Б. колеблется от 0,11 до 2,00 мг%. С помощью радиоактивного Б. (82Br) установлено избирательное поглощение его щитовидной железой, мозговым слоем почек и гипофизом. Введённые в организм животных и человека бромиды усиливают концентрацию процессов торможения в коре головного мозга, содействуют нормализации состояния нервной системы, пострадавшей от перенапряжения тормозного процесса. Одновременно, задерживаясь в щитовидной железе, Б. вступает в конкурентные отношения с Йодом, что влияет на деятельность железы, а в связи с этим — и на состояние обмена веществ.Лит.: Войнар А. И., Биологическая роль микроэлементов в организме животных и человека, 2 изд., М., 1960; Верховская И. Н., Бром в животном организме и механизм его действия, М., 1962.В. В. Ковальский.
с образованием бромистоводородной кислоты HBr и неустойчивой бромноватистой кислоты (См. Бромноватистая кислота) HBrO. Раствор Б. в воде называется бромной водой (См. Бромная вода). При растворении Б. в растворах щелочей на холоду происходит образование бромида и гипобромита (2NaOH + Br2 = NaBr + NaBrO + H2O), а при повышенных температурах (около 100°С) — бромида и бромата (6NaOH + 3Br2 = 5NaBr + NaBrO3 + ЗН2О). Из реакций Б. с органическими соединениями наиболее характерны присоединение по двойной связи С=С, а также замещение водорода (обычно при действии катализаторов или света).Получение и применение. Исходным сырьём для получения Б. служат морская вода, озёрные и подземные рассолы и щелока калийного производства, содержащие Б. в виде бромид-иона Br- (от 65 г/м3 в морской воде до 3—4 кг/м3 и выше в щелоках калийного производства). Б. выделяют при помощи хлора (2Вг- + Cl2 = Br2 + 2С1-) и отгоняют из раствора водяным паром или воздухом. Отгонку паром ведут в колоннах, изготовленных из гранита, керамики или иного стойкого к Б. материала. Сверху в колонну подают подогретый рассол, а снизу — хлор и водяной пар. Пары Б., выходящие из колонны, конденсируют в керамиковых холодильниках. Далее Б. отделяют от воды и очищают от примеси хлора дистилляцией. Отгонка воздухом позволяет использовать для получения Б. рассолы с его низким содержанием, выделять Б. из которых паровым способом в результате большого расхода пара невыгодно. Из получаемой бромовоздушной смеси Б. улавливают химическими поглотителями. Для этого применяют растворы бромистого железа (2 FeBr2 + Br2 = 2FeBr3), которое, в свою очередь, получают восстановлением FeBr3 железными стружками, а также растворы гидроокисей или карбонатов натрия или газообразный сернистый ангидрид, реагирующий с Б. в присутствии паров воды с образованием бромистоводородной и серной кислот (Br2 + 3O2 + 2H2O = 2HBr + H2SO4). Из полученных полупродуктов Б. выделяют действием хлора (из FeBr3 и HBr) или кислоты (5NaBr + NaBrO3 + 3Н2SO4 = 3Вr2 + 3Na2SO4 + 3Н2О). В случае необходимости полупродукты перерабатывают на бромистые соединения, не выделяя элементарного Б.Вдыхание паров Б. при содержании их в воздухе 1 мг/м3 и более вызывает кашель, насморк, носовое кровотечение, головокружение, головную боль; при более высоких концентрациях — удушье, бронхит, иногда смерть. Предельно допустимые концентрации паров Б. в воздухе 2 мг/м3. Жидкий Б. действует на кожу, вызывая плохо заживающие ожоги. Работы с Б. следует проводить в вытяжных шкафах. При отравлении парами Б. рекомендуется вдыхать аммиак, используя для этой цели сильно разбавленный раствор его в воде или в этиловом спирте. Боль в горле, вызванную вдыханием паров Б., устраняют приёмом внутрь горячего молока. Б., попавший на кожу, смывают большим количеством воды или сдувают сильной струей воздуха. Обожжённые места смазывают ланолином.Б. применяют довольно широко. Он — исходный продукт для получения ряда бромистых солей и органических производных. Большие количества Б. расходуют для получения бромистого этила и ди-бромэтана — составных частей этиловой жидкости, добавляемой к бензинам для повышения их детонационной стойкости (см. Антидетонаторы). Соединения Б. применяют в фотографии, при производстве ряда красителей, бромистый метил и некоторые другие соединения Б. — как инсектициды. Некоторые органические соединения Б. служат эффективными огнетушащими средствами. Б. и бромную воду используют при химических анализах для определения многих веществ. В медицине используют бромиды натрия, калия, аммония, а также органические соединения Б., которые применяют при неврозах, истерии, повышенной раздражительности, бессоннице, гипертонической болезни, эпилепсии и хорее.Лит.: Ксензенко В. И., Стасиневич Д. С., Технология брома и йода, М., 1960; Позин М. Е., Технология минеральных солей, 2 изд., Л., 1961; Bromine and its compounds, ed. Z. Е. Jolles, L., 1966.В. К. Бельский, Д. С. Стасиневич.Бром в организме. Б. — постоянная составная часть тканей животных и растений. Наземные растения содержат в среднем 7·10-4% Б. на сырое вещество, животные Бром1·10-4%/ Б. найден в различных секретах (слезах, слюне, поте, молоке, желчи). В крови здорового человека содержание Б. колеблется от 0,11 до 2,00 мг%. С помощью радиоактивного Б. (82Br) установлено избирательное поглощение его щитовидной железой, мозговым слоем почек и гипофизом. Введённые в организм животных и человека бромиды усиливают концентрацию процессов торможения в коре головного мозга, содействуют нормализации состояния нервной системы, пострадавшей от перенапряжения тормозного процесса. Одновременно, задерживаясь в щитовидной железе, Б. вступает в конкурентные отношения с Йодом, что влияет на деятельность железы, а в связи с этим — и на состояние обмена веществ.Лит.: Войнар А. И., Биологическая роль микроэлементов в организме животных и человека, 2 изд., М., 1960; Верховская И. Н., Бром в животном организме и механизм его действия, М., 1962.В. В. Ковальский.
Большая советская энциклопедия. — М.: Советская энциклопедия. 1969—1978.
